人教版九年级化学复习重点难点有哪些?
校园之窗 2026年1月18日 19:21:10 99ANYc3cd6
人教版九年级化学复习全攻略
复习的核心思路是:“回归课本,构建体系,突破重点,强化训练”。
第一部分:知识体系构建(搭建你的化学知识大厦)
九年级化学主要分为两大块:《化学》上册和《化学》下册,我们先从宏观上把握整体结构。

(图片来源网络,侵删)
《化学》上册 —— 化学启蒙与基础理论
这是化学的入门,也是整个化学的基石,必须学扎实。
| 单元 | 核心主题 | 核心知识点与考点 | 常见误区/易错点 |
|---|---|---|---|
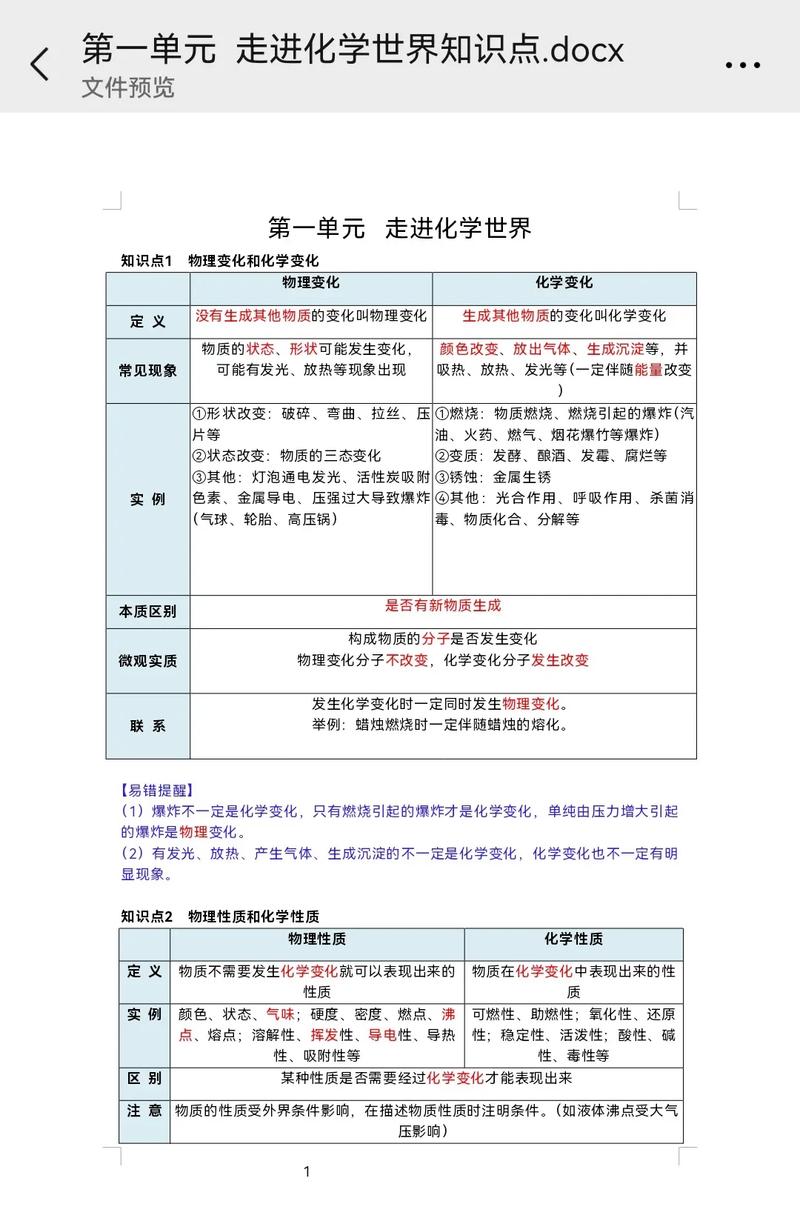
| 第一单元 走进化学世界 | 认识化学 化学实验基本操作 |
化学变化与物理变化的本质区别(是否有新物质生成)。 化学性质与物理性质的区别(是否需要通过化学变化体现)。 常用仪器的识别与用途(试管、烧杯、量筒、酒精灯、胶头滴管等)。 基本操作:药品取用、连接装置、检查装置气密性、加热、过滤、蒸发等。 |
判断变化时,只看现象(如发光、发热、变色),不看本质。 量筒读数时,俯视读数偏小,仰视读数偏大。 过滤操作中“一贴、二低、三靠”记不清。 |
| 第二单元 我们周围的空气 | 空气的成分 氧气性质与制备 化学反应类型 |
空气成分(体积分数):N₂ (78%), O₂ (21%), 稀有气体 (0.94%), CO₂ (0.03%)。 氧气的化学性质:支持燃烧(与C、S、P、Fe等反应)、供给呼吸。 氧气的实验室制法:药品(高锰酸钾、氯酸钾与MnO₂、过氧化氢溶液与MnO₂)、装置、收集方法(排水法/向上排空气法)、验满/检验方法。 化合反应、分解反应、氧化反应的概念与辨析。 |
混淆“纯净物”和“混合物”,如“洁净的空气”仍是混合物。 氧气化学性质描述不完整,如“铁在氧气中燃烧生成四氧化三铁”,而不是“氧化铁”。 催化剂“一变两不变”(改变反应速率,反应前后质量和化学性质不变)理解不透彻。 |
| 第三单元 物质构成的奥秘 | 【难点重点】 微观粒子 元素 物质分类 化学式与化合价 |
分子、原子、离子的关系与区别:分子由原子构成;原子得失电子变成离子;离子构成物质。 原子的结构:质子(+)、中子、核外电子(-),核电荷数=质子数=核外电子数(原子中)。 元素:具有相同核电荷数(即质子数)的一类原子的总称,元素符号、元素周期表。 物质分类:混合物 vs. 纯净物;单质 vs. 化合物;氧化物 vs. 化合物。 化学式:表示物质组成的意义,书写规则。 化合价:元素化合价规则(化合物中正负化合价代数和为零),化合价的应用(求未知元素化合价、书写化学式)。 |
分子是保持物质化学性质的最小微粒,原子是化学变化中的最小微粒。 元素讲的是“种类”,不讲个数;物质讲的是“种类”,不讲“个数”。 化合价是元素的一种性质,在化合物中才体现,单质中元素化合价为零。 化学式书写不规范,如把“H₂O”写成“HO₂”。 |
| 第四单元 自然界的水 | 水的净化 水的组成 化学方程式 |
水的净化:沉降、过滤、吸附、消毒,硬水与软水的区别及软化方法。 水的组成:电解水实验(正氧负氢,氢二氧一)。 质量守恒定律、微观解释(原子“三不变”)。 化学方程式:定义、书写原则(客观、守恒)、配平方法(观察法、最小公倍数法等)、读法。 |
过滤不能降低水的硬度,吸附和蒸馏可以。 电解水实验中,正负极产生的气体体积比是1:2,质量比是1:8。 化学方程式配平是重中之重,必须熟练掌握。 化学方程式中的“↑”、“↓”等标注符号使用不规范。 |
| 第五单元 化学方程式 | 【核心计算】 质量守恒定律的应用 根据化学方程式的计算 |
质量守恒定律的应用:推断未知物、求反应物/生成物的质量差。 计算类型: - 已知一种纯净物的质量,求另一种纯净物的质量。 - 含杂质(不纯)物质的计算(注意:必须换算成纯净物的质量)。 - 与溶液的综合计算。 |
计算时忘记将不纯物质的质量换算成纯净物的质量。 化学方程式未配平就进行计算。 计算过程不规范,单位不统一。 |
| 第六单元 碳和碳的氧化物 | 碳的单质 二氧化碳和一氧化碳 |
碳的单质:金刚石、石墨、C₆₀的结构与性质差异(物理性质不同,化学性质相似)。 碳的化学性质:常温下稳定,高温下可燃性和还原性。 CO₂的实验室制法:药品(大理石/石灰石与稀盐酸)、装置、收集方法(向上排空气法)、检验方法。 CO₂的性质:不燃烧不支持燃烧、与水反应、与石灰水反应。 CO的性质:可燃性、还原性、剧毒性。 |
混淆碳和几种碳单质的性质,尤其是物理性质。 CO₂和石灰水反应的原理用于检验CO₂,但长期通入会使石灰水变浑浊后又变澄清。 CO的毒性原理(与血液中的血红蛋白结合)和还原性(与CuO等反应)是考点。 |
| 第七单元 燃料及其利用 | 燃烧与灭火 能源与环保 |
燃烧的条件:可燃物、氧气(或空气)、达到着火点(三者缺一不可)。 灭火的原理:破坏任意一个燃烧条件。 化石燃料:煤、石油、天然气(主要成分是甲烷CH₄)。 化学反应中的能量变化:放热反应(如燃烧)和吸热反应。 使用燃料对环境的影响:酸雨、温室效应等。 |
着火点是物质本身的固有属性,不能降低,只能使温度降低到着火点以下。 燃烧不一定需要氧气,如镁在CO₂中可以燃烧。 甲烷、乙醇等物质的化学式、燃烧方程式要记牢。 |
《化学》下册 —— 生活中常见的化合物与酸碱盐
这部分是化学的重点和难点,内容多、杂、乱,但规律性强,需要分类归纳。
| 单元 | 核心主题 | 核心知识点与考点 | 常见误区/易错点 |
|---|---|---|---|
| 第八单元 金属和金属材料 | 金属的性质 金属活动性顺序 |
金属的物理性质:导电性、导热性、延展性等。 金属的化学性质: - 与O₂反应(大多数金属)。 - 与酸反应(排在H前的金属)。 - 与盐溶液反应(“前置后”)。 金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au。 金属活动性顺序的应用:判断反应能否发生、判断金属活动性强弱、判断溶液质量变化。 |
铁与酸、盐溶液反应生成的是亚铁盐(Fe²⁺),不是铁盐(Fe³⁺)。 “K Ca Na Na Ca K”太活泼,不能直接与盐溶液反应,会先与水反应。 金属活动性顺序是判断置换反应能否发生的核心依据,必须熟记。 |
| 第九单元 溶液 | 【核心计算】 溶液的形成 溶解度 溶质的质量分数 |
溶液的概念:均一、稳定的混合物,溶质、溶剂的判断。 饱和溶液与不饱和溶液的转化方法。 溶解度:四要素(温度、100g溶剂、饱和状态、单位是g)。 溶解度曲线的意义与应用(比较溶解度大小、判断溶解度随温度变化趋势、查找某温度下的溶解度、结晶方法)。 溶质的质量分数:定义、计算公式。 溶液的稀释与配制:稀释前后溶质质量不变。 |
溶液不一定是无色的,如CuSO₄溶液是蓝色的。 饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。 溶解度曲线的“交点”表示在该温度下两物质的溶解度相等。 溶液配制中,仰视/俯视量筒读数、烧杯未冷却就称量质量是常见错误。 |
| 第十单元 酸和碱 | 【核心重点】 常见的酸和碱 酸碱的化学性质 中和反应 |
常见的酸:盐酸、硫酸的物理性质和化学性质(通性)。 常见的碱:氢氧化钠、氢氧化钙的物理性质和化学性质(通性)。 酸碱指示剂:酚酞(遇酸不变,遇碱变红)、石蕊(遇酸变红,遇碱变蓝)。 中和反应:酸和碱作用生成盐和水的反应,应用(改良土壤、处理废水、医药等)。 溶液的酸碱度:pH(0-14),pH<7酸性,pH=7中性,pH>7碱性。 |
浓硫酸的稀释(“酸入水”)和氢氧化钠的潮解、腐蚀性。 酸碱的化学性质繁多,要系统归纳,形成网络图。 中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应(如CuO + H₂SO₄)。 pH的测定方法(玻璃棒蘸取,比色卡)。 |
| 第十一单元 盐 化肥 | 【综合难点】 常见的盐 复分解反应 化学肥料 |
常见的盐:氯化钠、碳酸钠、碳酸氢钠的俗称、性质和用途。 粗盐提纯:溶解、过滤、蒸发。 复分解反应:定义、发生的条件(生成沉淀、气体或水)。 离子的检验:Cl⁻(用AgNO₃和稀HNO₃)、SO₄²⁻(用BaCl₂和稀HNO₃)、CO₃²⁻(用稀盐酸和澄清石灰水)。 化肥:氮肥、磷肥、钾肥的作用和鉴别。 |
盐的化学性质与酸、碱的化学性质相互关联,要融会贯通。 复分解反应的条件是“生成物中有沉淀、气体或水”,缺一不可。 离子检验中,滴加稀硝酸是为了排除其他离子的干扰(如CO₃²⁻对Cl⁻检验的干扰)。 |
| 第十二单元 化学与生活 | 人类重要的营养物质 化学元素与人体健康 有机合成材料 |
六大营养素:蛋白质、糖类、油脂、维生素、无机盐、水。 元素与人体健康:Ca、Fe、I、Zn、Se等元素的作用及缺乏症。 有机物与无机物的区别。 三大合成材料:塑料、合成纤维、合成橡胶。 |
区分“营养素”和“元素”,如缺钙会得骨质疏松症,这里的“钙”指元素。 了解常见物质的分类(如淀粉、蛋白质是有机物)。 区分“天然材料”和“合成材料”。 |
第二部分:高效复习策略与方法
光有知识框架还不够,科学的方法能让你的复习事半功倍。
-
回归课本,夯实基础
 (图片来源网络,侵删)
(图片来源网络,侵删)- 做什么:从头到尾快速阅读课本,特别是黑体字、定义、实验步骤、化学方程式、图片和注释,把课本上的每一个知识点都过一遍。
- 怎么做:准备一个“错题本”和“好题本”,将课本上重要的概念、定义、方程式抄录下来,反复记忆。
-
专题突破,攻克难点
- 做什么:将知识体系中的“难点重点”和“核心计算”单独拿出来,进行专项训练。
- 怎么做:
- 酸碱盐:这是重中之重,自己动手画一张“酸碱盐相互关系图”,梳理它们之间的反应规律。
- 化学计算:把上册的“质量守恒”和下册的“溶质质量分数”计算题分类整理,每种题型找5-10道经典题目反复练习,直到掌握解题模板。
- 实验探究:将所有实验(制O₂、CO₂、电解水、粗盐提纯等)的目的、药品、装置、步骤、现象、注意事项进行对比总结。
-
建立错题本,查漏补缺
- 做什么:这是最有效的提分方法!把平时作业、练习、考试中所有做错的题都整理到错题本上。
- 怎么做:
- 抄题:完整抄下原题。
- 写错解:写下你当时的错误解法。
- 写正解:写出正确的解题过程和答案。
- 写反思:分析错误原因(概念不清?计算失误?审题不清?),并注明涉及的知识点。
- 定期回顾:每周、考前都要翻看错题本,确保同样的错误不再犯第二次。
-
回归真题,模拟实战
- 做什么:在复习后期,一定要用中考真题或高质量的模拟题进行实战演练。
- 怎么做:
- 掐时训练:严格按照中考时间(通常是60-70分钟)完成一套试卷,锻炼时间分配能力。
- 分析试卷:做完后认真批改,分析失分点,是哪个模块的知识薄弱,是计算粗心还是审题不清。
- 总结规律:研究近几年本地中考化学的题型、分值分布、高频考点,做到心中有数。
第三部分:考前冲刺与应试技巧
- 回归基础,回归错题:考前一周不要再做新题、难题,把课本目录过一遍,确保每个知识点都有印象,把错题本看几遍,这是你的“宝藏”。
- 调整心态,保证睡眠:保持自信,相信自己平时的努力,考前保证充足睡眠,让大脑在考场上处于最佳状态。
- 应试技巧:
- 通览全卷,心中有数:花2-3分钟快速浏览全卷,了解题量、题型和难度,合理分配时间。
- 先易后难,稳扎稳打:从有把握的题目做起,建立信心,遇到难题暂时跳过,做好标记,最后再攻克。
- 审题要慢,答题要快:圈出题目中的关键词(如“正确的是”、“不包含”、“过量”),避免因审题失误丢分。
- 书写规范,卷面整洁:化学用语(元素符号、化学式、方程式)要书写规范,字迹清晰,计算题步骤要完整。
- 不留空白,绝不放弃:即使不会做的题,也要根据所学知识写一些相关的化学方程式或概念,争取步骤分。
送你一句话:化学不难,在于“格物致知”。

(图片来源网络,侵删)
只要你肯花时间,肯动脑筋,把零散的知识点串成线、连成网,化学世界的大门就会为你敞开,祝你复习顺利,中考取得优异成绩!加油!










