人教版九年级化学知识点总结有哪些重点?
校园之窗 2025年12月9日 05:26:07 99ANYc3cd6
人教版九年级化学全册知识点总结
第一单元 走进化学世界
核心主题: 认识化学,学习化学的基本方法——科学探究。
化学是一门以实验为基础的科学

- 化学研究的对象: 物质的组成、结构、性质以及变化规律。
- 化学变化与物理变化的根本区别: 是否有新物质生成。
- 物理变化: 没有新物质生成,如:水的三态变化、石蜡熔化。
- 化学变化(化学反应): 有新物质生成,如:燃烧、生锈、食物腐败。
- 现象: 化学变化常伴随发光、放热、变色、产生气体、生成沉淀等现象,但不能仅凭现象判断,关键看有无新物质。
- 物理性质与化学性质
- 物理性质: 不需要发生化学变化就表现出来的性质,如:颜色、状态、气味、熔点、沸点、硬度、密度、溶解性、挥发性等。
- 化学性质: 物质在化学变化中表现出来的性质,如:可燃性、助燃性、氧化性、还原性、酸性、碱性等。
化学是一门以实验为基础的科学
- 常用仪器及使用:
- 反应容器: 试管、烧杯、锥形瓶、烧瓶、蒸发皿。
- 量取仪器: 量筒(不能加热,不能作反应容器,读数时视线与凹液面最低处保持水平)。
- 加热仪器: 酒精灯(“三禁止”:禁止向燃着的酒精灯添加酒精;禁止用燃着的酒精灯去点燃另一只;禁止用嘴吹灭,要用灯帽盖灭)。
- 夹持仪器: 试管夹、铁架台(含铁夹、铁圈)。
- 其他: 胶头滴管、玻璃棒、药匙、水槽、集气瓶。
- 基本操作:
- 药品取用:
- “三不”原则:不闻、不尝、不直接接触。
- 液体:少量用胶头滴管,较多用倾倒法(标签对手心)。
- 固体:块状用镊子(“一横二放三慢竖”),粉末用药匙或纸槽(“一斜二送三直立”)。
- 物质的加热:
- 酒精灯火焰分:外焰(温度最高)、内焰、焰心。
- 加热固体:试管口略向下倾斜,防止冷凝水倒流炸裂试管。
- 加热液体:试管倾斜约45°,试管口不能对着任何人,防止液体沸腾喷出伤人。
- 仪器的连接与洗涤:
- 连接玻璃导管和橡皮管:先用水润湿,然后稍用力转动插入。
- 检查装置气密性:将导管末端浸入水中,双手紧贴容器外壁,若导管口有气泡冒出,松开手后形成一段水柱,则气密性良好。
- 仪器洗涤:洗净的标准是内壁附着的水既不聚成水滴,也不成股流下。
- 药品取用:
第二单元 我们周围的空气
核心主题: 空气的成分,氧气的性质、制法和用途。
空气的成分
- 体积分数:
- 氮气(N₂):约 78%
- 氧气(O₂):约 21%
- 稀有气体:约 0.94%
- 二氧化碳(CO₂):约 0.03%
- 其他气体和杂质:约 0.03%
- 氧气含量的测定实验(拉瓦锡实验):
- 原理: 红磷燃烧消耗氧气,导致瓶内压强减小,水倒吸入集气瓶,倒吸入水的体积约等于氧气的体积。
- 现象: 红磷燃烧,产生大量白烟;冷却后,打开止水夹,水倒流入集气瓶,约占瓶内气体体积的1/5。
- 氧气约占空气体积的1/5。
- 成功关键: 装置气密性良好;红磷要过量;冷却至室温后再打开止水夹。
氧气(O₂)

- 物理性质: 无色无味的气体,不易溶于水,密度比空气略大(可用向上排空气法收集)。
- 化学性质(氧化性):
- 与木条(带火星): 木条复燃(检验氧气)。
- 与硫: 在空气中发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰,生成有刺激性气味的气体(SO₂)。
- 与铁: 在氧气中剧烈燃烧,火星四射,生成黑色固体(Fe₃O₄),此实验在集气瓶底铺一层细沙或水,防止高温熔融物炸裂瓶底。
- 与镁: 发出耀眼白光,生成白色固体(MgO)。
- 与石蜡: 发出白光,瓶壁有水雾,生成使澄清石灰水变浑浊的气体(CO₂)。
- 用途: 供给呼吸(潜水、医疗)、支持燃烧(炼钢、气焊)。
- 制法:
- 工业制法: 分离液态空气法(物理变化,利用液氮和液氧的沸点不同)。
- 实验室制法:
- 药品: 过氧化氢(H₂O₂)和二氧化锰(MnO₂) / 高锰酸钾(KMnO₄) / 氯酸钾(KClO₃)和二氧化锰(MnO₂)。
- 反应原理:
2H₂O₂ --(MnO₂)--> 2H₂O + O₂↑2KMnO₄ --(加热)--> K₂MnO₄ + MnO₂ + O₂↑(试管口要放一团棉花)2KClO₃ --(MnO₂, 加热)--> 2KCl + 3O₂↑
- 发生装置: 固体加热型(高锰酸钾、氯酸钾)或 固液不加热型(过氧化氢)。
- 收集装置: 排水法(因为O₂不易溶于水)或 向上排空气法(因为O₂密度比空气大)。
- 检验: 将带火星的木条伸入集气瓶,木条复燃,则是氧气。
- 验满:
- 排水法:当集气瓶口有大气泡冒出时,已收集满。
- 向上排空气法:将带火星的木条放在集气瓶口,木条复燃,已收集满。
催化剂与催化作用
- 定义: 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有变化的物质。
- 特点: “一变两不变”——改变速率、质量不变、化学性质不变。
- 注意: 催化剂不一定只有加快速率的作用,也可能减慢。
第三单元 物质构成的奥秘
核心主题: 从微观角度认识物质的构成。
分子和原子
- 分子: 保持物质化学性质的最小粒子,在化学变化中,分子可以再分。
- 原子: 化学变化中的最小粒子,在化学变化中,原子不可再分。
- 关系: 分子由原子构成,原子可以构成分子,也可以直接构成物质(如金属、稀有气体)。
- 用分子的观点解释现象:
- 物理变化: 分子本身没有改变,分子间隔发生了改变。
- 化学变化: 分子分裂成原子,原子重新组合成新分子。
- 三态变化: 主要是分子间隔不同造成的。
原子的构成
- 结构: 原子由原子核(带正电)和核外电子(带负电)构成,原子核由质子(带正电)和中子(不带电)构成。
- 关系:
核电荷数 = 质子数 = 核外电子数(原子中)相对原子质量 ≈ 质子数 + 中子数
- 核外电子的排布:
- 电子在核外分层排布,能量低的离核近,能量高的离核远。
- 原子结构示意图: 圆圈表示原子核,+号表示核电荷数,弧线表示电子层,数字表示该层电子数。
元素
- 定义: 质子数(即核电荷数)相同的一类原子的总称。
- 地壳中元素含量排名: 氧、硅、铝、铁。
- 元素符号:
- 国际通用,由一个或两个字母表示。
- 书写原则:“一大二小”,如:H、He、Na、Ca。
- 元素周期表:
- 周期: 横行,共有7个周期。
- 族: 纵行,共有18个族。
- 原子序数 = 核电荷数 = 质子数 = 核外电子数。
离子
- 定义: 带电荷的原子或原子团。
- 形成: 原子得电子形成阴离子(带负电),失电子形成阳离子(带正电)。
- 表示方法: 在元素符号右上角标出电荷数和电性,如:Na⁺、Cl⁻、SO₄²⁻。
化学式与化合价
- 化学式: 用元素符号和数字的组合表示物质组成的式子。
- 意义:
- 宏观:表示一种物质;表示该物质的元素组成。
- 微观:表示该物质的一个分子;表示一个分子的构成。
- H₂O 表示水;水由氢、氧元素组成;一个水分子;一个水分子由2个氢原子和1个氧原子构成。
- 写法与读法:
- 单质:O₂、Fe、He。
- 化合物:氧化物(氧在后,如CO₂);金属与非金属(金属在前,非金属在后,如NaCl)。
- 意义:
- 化合价:
- 规则: 化合物中正负化合价代数和为零。
- 常见元素化合价口诀:
- 钾钠银氢正一价,钙镁钡锌正二价。
- 氧通常显负二价,氯通常显负一价。
- 硫有负二正四六,碳有正二和正四。
- 铜汞二价最常见,铝正三来铁正二三。
- 应用: 根据化合价书写化学式(十字交叉法);根据化学式计算某元素化合价。
有关化学式的计算
- 相对分子质量 = 各原子的相对原子质量 × 原子个数之和
- 各元素质量比 = 各原子的相对原子质量 × 原子个数之比
- 某元素的质量分数 = (该元素的相对原子质量 × 原子个数 / 相对分子质量) × 100%
第四单元 自然界的水
核心主题: 水的组成、净化和爱护水资源。
水的组成
- 电解水实验:
- 现象: 正极(O₂)产生气体少,负极(H₂)产生气体多,体积比约为 1:2。
- 水是由氢、氧两种元素组成的,化学方程式:
2H₂O --(通电)--> 2H₂↑ + O₂↑ - 正负极气体检验: 正极:用带火星的木条,木条复燃(O₂);负极:点燃,气体燃烧,产生淡蓝色火焰(H₂)。
单质与化合物
- 单质: 由同种元素组成的纯净物,如:O₂、H₂、Fe。
- 化合物: 由不同种元素组成的纯净物,如:H₂O、CO₂、KClO₃。
- 氧化物: 由两种元素组成,其中一种是氧元素的化合物,如:H₂O、CO₂、Fe₃O₄。
水的净化
- 步骤: 沉淀 → 过滤 → 吸附 → 消毒。
- 硬水与软水:
- 硬水: 含有较多可溶性钙、镁化合物的水。
- 软水: 不含或含较少可溶性钙、镁化合物的水。
- 检验: 加入肥皂水,泡沫多、浮渣少的是软水;泡沫少、浮渣多的是硬水。
- 硬水软化: 生活中煮沸,实验室和工业上蒸馏。
- 蒸馏: 净化程度最高的方法,得到的是蒸馏水。
爱护水资源
- 措施: 一方面要节约用水,另一方面要防治水体污染。
- 水污染来源: 工业废水、农业污染、生活污水。
第五单元 化学方程式
核心主题: 质量守恒定律,化学方程式的书写与计算。
质量守恒定律
- 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
- 微观解释: 化学反应前后,原子的种类、数目、质量均不改变。
- “五个不改变,两个一定改变,一个可能改变”:
- 不改变:原子种类、原子数目、原子质量、元素种类、物质总质量。
- 一定改变:分子种类、物质种类。
- 可能改变:分子数目。
化学方程式的书写
- 原则: 以客观事实为基础;遵守质量守恒定律。
- 步骤: 写(反应物、生成物)→ 配(配平)→ 标(条件、↑↓)→ 等(短线改等号)。
- 配平方法: 最小公倍数法、观察法、奇数配偶法。
根据化学方程式的计算
- 步骤:
- 设: 设未知量。
- 写: 写出正确的化学方程式。
- 找: 找出相关物质的相对分子质量,已知量和未知量。
- 列: 列出比例式。
- 求: 求解。
- 答: 简明写出答案。
- 注意事项:
- 代入方程式计算的量必须是纯净物的质量。
- 若不纯,需先换算成纯净物质量:纯净物质量 = 混合物质量 × 纯度。
- 单位要统一。
第六单元 碳和碳的氧化物
核心主题: 碳的单质及其氧化物。
碳的单质
- 金刚石、石墨、C₆₀:
- 共同点: 都是由碳元素组成的单质;物理性质差异大是因为碳原子排列方式不同。
- 金刚石: 自然界最硬的物质,用于切割玻璃、钻头。
- 石墨: 质软,有滑腻感,有优良的导电性,用于电极、铅笔芯。
- C₆₀: 由分子构成的,形似足球。
- 无定形碳: 木炭、活性炭、焦炭、炭黑,它们都具有疏松多孔的结构,有吸附性(物理性质)。
- 碳的化学性质:
- 常温下: 稳定。
- 点燃时: 可燃性
- 充分燃烧:
C + O₂ --(点燃)--> CO₂(放热多) - 不充分燃烧:
2C + O₂ --(点燃)--> 2CO
- 充分燃烧:
- 高温下: 还原性
C + 2CuO --(高温)--> 2Cu + CO₂↑(黑色粉末变红色,澄清石灰水变浑浊)3C + 2Fe₂O₃ --(高温)--> 4Fe + 3CO₂↑
二氧化碳(CO₂)
- 物理性质: 无色无味气体,密度比空气大,能溶于水,固体叫“干冰”,易升华吸热。
- 化学性质:
- 不能燃烧,不支持燃烧(一般情况下)。
- 与水反应:
CO₂ + H₂O == H₂CO₃(碳酸不稳定,易分解:H₂CO₃ == H₂O + CO₂↑) - 与碱反应(检验CO₂):
CO₂ + Ca(OH)₂ == CaCO₃↓ + H₂O(澄清石灰水变浑浊)。 - 与灼热的碳反应:
CO₂ + C --(高温)--> 2CO
- 用途: 灭火、制冷剂(干冰)、人工降雨、化工原料。
- 实验室制法:
- 药品: 石灰石(或大理石)和稀盐酸。
- 原理:
CaCO₃ + 2HCl == CaCl₂ + H₂O + CO₂↑ - 发生装置: 固液不加热型。
- 收集装置: 向上排空气法(因为CO₂密度比空气大,且能溶于水)。
- 检验: 将气体通入澄清石灰水中,石灰水变浑浊。
- 验满: 将燃着的木条放在集气瓶口,木条熄灭。
一氧化碳(CO)
- 物理性质: 无色无味气体,密度比空气略小,难溶于水。
- 化学性质:
- 可燃性:
2CO + O₂ --(点燃)--> 2CO₂(蓝色火焰) - 毒性: 与血液中的血红蛋白结合,使人体缺氧。
- 还原性:
CO + CuO --(加热)--> Cu + CO₂(黑色粉末变红色)
- 可燃性:
- CO与CO₂的鉴别与除杂:
- 鉴别:
- 通入澄清石灰水,变浑浊的是CO₂。
- 点燃,能燃烧的是CO。
- 通过灼热的CuO,黑色变红色,生成气体使石灰水变浑浊的是CO。
- 除杂:
- 除去CO中的CO₂:通过足量NaOH溶液。
- 除去CO₂中的CO:通过灼热的CuO。
- 鉴别:
第七单元 燃料及其利用
核心主题: 燃烧与灭火,能源的利用与开发。
燃烧与灭火
- 燃烧条件(三者缺一不可):
- 可燃物
- 氧气(或空气)
- 达到燃烧所需的最低温度(着火点)
- 灭火原理(破坏任意一个条件即可):
- 清除可燃物或使可燃物与其他物品隔离。
- 隔绝氧气(或空气)。
- 使温度降到着火点以下。
- 爆炸: 可燃物在有限的空间内急速燃烧,在短时间内产生大量的热,使气体体积急剧膨胀而引起的。
燃料与热量
- 化石燃料: 煤、石油、天然气(都是混合物)。
- 煤: 主要含碳元素,被称为“工业的粮食”。
- 石油: 主要含碳、氢元素,被称为“工业的血液”。
- 天然气: 主要成分是甲烷(CH₄)。
- 甲烷性质: 无色无味气体,密度比空气小,极难溶于水,燃烧方程式:
CH₄ + 2O₂ --(点燃)--> CO₂ + 2H₂O
- 甲烷性质: 无色无味气体,密度比空气小,极难溶于水,燃烧方程式:
- 化学反应中的能量变化:
- 放热反应:如燃烧、中和反应、活泼金属与酸反应。
- 吸热反应:如碳与二氧化碳的反应、碳酸盐与酸的反应。
使用燃料对环境的影响
- 空气污染物: 二氧化硫、二氧化氮、一氧化碳、可吸入颗粒物。
- 酸雨: 由二氧化硫、二氧化氮等气体溶于雨水形成。
- 能源与可持续发展:
- 清洁能源:氢能、太阳能、风能、地热能。
- 乙醇(C₂H₅OH):属于可再生能源,燃烧产物是水和二氧化碳,比较清洁。
第八单元 金属和金属材料
核心主题: 金属的物理性质、化学性质、冶炼及资源保护。
金属的物理性质
- 共性: 有金属光泽、导电性、导热性、延展性。
- 特性: 大多数呈银白色(铜为紫红色,金为黄色);常温下为固体(汞为液体);密度、硬度、熔点各不相同。
合金
- 定义: 在金属中加热熔合某些金属或非金属,形成的具有金属特性的物质。
- 常见合金:
- 铁合金:生铁(含碳量2%-4.3%)、钢(含碳量0.02%-2%)。
- 铜合金:黄铜(铜锌合金)、青铜(铜锡合金)。
- 特性: 合金的硬度大、熔点低,性能优于纯金属。
金属的化学性质
- 与氧气反应:
4Al + 3O₂ --(加热)--> 2Al₂O₃(致密氧化膜,抗腐蚀)3Fe + 2O₂ --(点燃)--> Fe₃O₄2Cu + O₂ --(加热)--> 2CuO
- 与酸反应(金属活动性H前的金属):
Zn + H₂SO₄ == ZnSO₄ + H₂↑Fe + 2HCl == FeCl₂ + H₂↑(亚铁盐,溶液为浅绿色)
- 与盐溶液反应(活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来):
Fe + CuSO₄ == FeSO₄ + Cu(铁丝表面附着一层红色物质,溶液由蓝色变为浅绿色)Cu + 2AgNO₃ == Cu(NO₃)₂ + 2Ag(铜丝表面附着一层银白色物质)
金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 钾钙钠镁铝、锌铁锡铅氢、铜汞银铂金
- 意义:
- 排H前的金属能与酸反应生成氢气。
- 排在前面的金属能把排在后面的金属从其盐溶液中置换出来(K、Ca、Na除外,它们会先与水反应)。
金属资源的利用与保护
- 铁的冶炼:
- 原料: 铁矿石、焦炭、石灰石、空气。
- 原理: 在高温下,利用一氧化碳将铁从铁矿石中还原出来。
3CO + Fe₂O₃ --(高温)--> 2Fe + 3CO₂
- 铁的锈蚀与防护:
- 条件: 与氧气、水同时接触。
- 防锈方法: 保持表面洁净干燥;形成保护膜(如涂油、刷漆、电镀、制成不锈钢)。
- 金属资源保护: 防止腐蚀;回收利用;有计划、合理地开采矿物。
第九单元 溶液
核心主题: 溶液的形成、溶解度及溶质质量分数的计算。
溶液的形成
- 定义: 一种或几种物质分散到另一种物质中,形成均一、稳定的混合物。
- 特征: 均一性、稳定性。
- 组成: 溶质(被溶解的物质)、溶剂(能溶解其他物质的物质),水是最常见的溶剂。
- 溶解过程中的热效应:
- 放热: NaOH、浓H₂SO₄溶解。
- 吸热: NH₄NO₃溶解。
- 温度不变: NaCl溶解。
饱和溶液与不饱和溶液
- 定义:
- 饱和溶液: 在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能再溶解时,所得到的溶液。
- 不饱和溶液: 还能继续溶解某种溶质的溶液。
- 相互转化:
- 饱和溶液 ⇌ 不饱和溶液
- 增加溶质或升高温度(多数物质) → 饱和 → 不饱和
- 增加溶剂或降低温度或增加溶质 → 不饱和 → 饱和
- 饱和溶液 ⇌ 不饱和溶液
溶解度
- 固体溶解度: 在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
- 四要素:温度、100g溶剂、饱和状态、质量(单位:克)。
- 溶解度曲线:
- 交点: 表示在该温度下,两种物质的溶解度相等。
- 曲线下方: 不饱和溶液。
- 曲线上方: 饱和溶液,且有未溶解的固体。
- 气体的溶解度: 在压强为101kPa和一定温度下,1体积水里溶解达到饱和状态时的气体体积。
- 影响因素:温度(温度升高,溶解度减小)、压强(压强增大,溶解度增大)。
溶质的质量分数
- 定义: 溶质质量与溶液质量之比。
- 公式:
w = (溶质质量 / 溶液质量) × 100%溶液质量 = 溶质质量 + 溶剂质量
- 一定溶质质量分数的氯化钠溶液的配制:
- 仪器: 托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管。
- 步骤: 计算 → 称量 → 量取 → 溶解(玻璃棒作用:搅拌,加速溶解)。
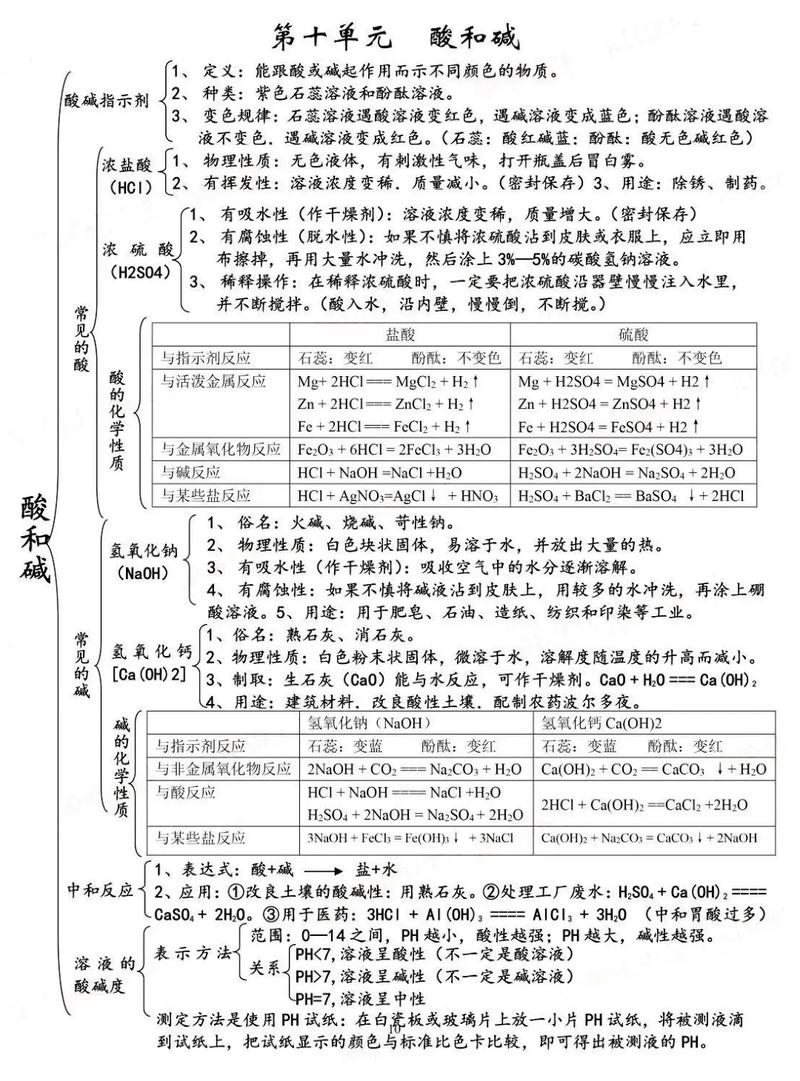
第十单元 酸和碱
核心主题: 常见的酸和碱的性质、用途及中和反应。
常见的酸
- 盐酸: 氯化氢气体的水溶液,易挥发,有刺激性气味。
- 硫酸: 纯硫酸是无色、粘稠、油状的液体,不易挥发,有吸水性(可作干燥剂)和脱水性。
- 酸的通性(H⁺的性质):
- 使紫色石蕊试液变红,无色酚酞不变色。
- 与活泼金属反应生成盐和氢气。
- 与金属氧化物反应生成盐和水(除锈)。
- 与碱发生中和反应生成盐和水。
- 与某些盐反应生成新酸和新盐。
常见的碱
- 氢氧化钠: 俗称烧碱、火碱、苛性钠,易潮解,有强烈的腐蚀性,可作干燥剂。
- 氢氧化钙: 俗称熟石灰、消石灰,微溶于水,水溶液叫石灰水。
- 碱的通性(OH⁻的性质):
- 使紫色石蕊试液变蓝,无色酚酞变红。
- 与非金属氧化物反应生成盐和水。
- 与酸发生中和反应生成盐和水。
- 与某些盐反应生成新碱和新盐。
中和反应
- 定义: 酸与碱作用生成盐和水的反应。
HCl + NaOH == NaCl + H₂O
- 应用: 改良土壤酸性、处理工厂废水、医药(如胃酸过多)。
溶液的酸碱度——pH
- pH范围: 0 ~ 14
- pH = 7,溶液呈中性。
- pH < 7,溶液呈酸性,pH越小,酸性越强。
- pH > 7,溶液呈碱性,pH越大,碱性越强。
- 测定: 用pH试纸。
- 方法: 在玻璃片上放一片pH试纸,用玻璃棒蘸取待测液滴在pH试纸上,将显示的颜色与标准比色卡对照。
- 注意: 不能将pH试纸直接伸入待测液中,也不能将pH试纸润湿。
第十一单元 盐 化肥
核心主题: 常见的盐、化学肥料及粗盐提纯。
生活中常见的盐
- 氯化钠: 俗称食盐,生理盐水是0.9%的NaCl溶液。
- 碳酸钠(Na₂CO₃): 俗称纯碱、苏打,水溶液呈碱性。
- 碳酸氢钠(NaHCO₃): 俗称小苏打,受热易分解,可作发酵粉。
- 碳酸钙(CaCO₃): 大理石、石灰石的主要成分,难溶于水。
盐的化学性质
- 与某些金属反应。
- 与酸反应。
- 与碱反应(复分解反应)。
- 与某些盐反应(复分解反应)。
复分解反应
- 定义: 两种化合物相互交换成分,生成另外两种新化合物的反应。
AB + CD → AD + CB
- 发生条件: 生成物中有沉淀、气体或水。
粗盐提纯
- 步骤: 溶解 → 过滤 → 蒸发。
- 玻璃棒的作用:
- 溶解时:搅拌,加速溶解。
- 过滤时:引流。
- 蒸发时:搅拌,防止局部温度过高造成液滴飞溅。
化学肥料
- 氮肥: 作用是促进植物茎、叶生长茂盛,叶色浓绿,如:NH₄HCO₃、NH₄NO₃。
- 磷肥: 作用是促进植物根系发达,增强抗寒抗旱能力,如:Ca₃(PO₄)₂。
- 钾肥: 作用是促进植物生长健壮,茎秆粗硬,增强抗病虫害和倒伏能力,如:K₂SO₄。
- 复合肥料: 含有两种或两种以上营养元素的肥料,如:KNO₃、NH₄H₂PO₄。
第十二单元 化学与生活
核心主题: 人类重要的营养物质、化学元素与健康、有机合成材料。
人类重要的营养物质
- 蛋白质: 是构成细胞的基本物质,是机体生长及修补受损组织的主要原料,遇到浓硝酸会变黄。
- 糖类: 是人类食物的主要成分,由C、H、O组成,如:淀粉、葡萄糖(C₆H₁₂O₆)。
- 油脂: 提供人体日所需能量的20%-25%。
- 维生素: 调节新陈代谢、预防疾病,缺乏维生素C会患坏血病。
化学元素与健康
- 常量元素: O、C、H、N、Ca、P、K、S、Na、Cl、Mg(占99.95%)。
- 微量元素: Fe(缺铁性贫血)、Zn(食欲不振,发育不良)、Se(防癌)、I(甲状腺肿大)、F(龋齿)。
有机合成材料
- 有机化合物: 含碳元素的化合物(CO、CO₂、碳酸盐等除外)。
- 高分子材料:
- 天然有机高分子材料: 棉花、羊毛、天然橡胶。
- 合成有机高分子材料(三大合成材料): 塑料、合成纤维、合成橡胶。
- “白色污染”: 指废弃塑料对环境造成的污染,防治措施:减少使用、重复使用、使用可降解塑料、回收利用。
中考高频考点与备考建议
- 化学用语: 元素符号、化学式、离子符号、化合价、化学方程式,这是化学的“语言”,必须滚瓜烂熟。
- 基本概念与理论: 物理变化与化学变化、分子与原子、质量守恒定律、溶液的定义与特征、酸碱盐的定义。
- 化学实验:
- 气体制备: O₂、CO₂、H₂的发生装置、收集方法、检验、验满。
- 物质检验与鉴别: O₂、CO₂、H₂、H₂O、酸、碱、盐。
- 基本操作:










