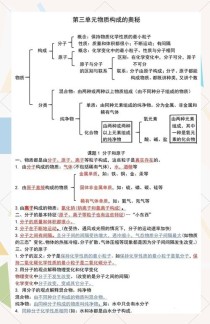
九年级化学上册第四单元的核心知识点是什么?
校园之窗 2025年12月18日 21:44:42 99ANYc3cd6
第四单元 物质构成的奥秘
核心思想
本单元的核心思想是:从微观粒子的角度认识物质的构成、性质和变化,我们将学习三种基本的微观粒子:分子、原子、离子,并理解它们之间的关系。
第一部分:原子的构成
这是本单元的基础,也是中考的必考点。

(图片来源网络,侵删)
原子的发现史(了解即可,有助于理解)
- 道尔顿:提出原子论,认为原子是实心球体,不可再分。(这是近代化学的开端)
- 汤姆生:发现了电子,提出了“葡萄干面包式”模型,认为原子中存在带负电的电子。
- 卢瑟福:通过α粒子散射实验,提出了核式结构模型(类似于太阳系),认识到原子是由原子核和核外电子构成的,原子核带正电,质量主要集中在原子核上。
原子的构成(核心知识点)
一个原子由两部分构成:
| 构成部分 | 位置 | 电性 | 质量 |
|---|---|---|---|
| 原子核 | 原子中心 | 带正电 (+) | 集中了原子的几乎全部质量 |
| 核外电子 | 原子核外高速运动 | 带负电 (-) | 质量很小,约为质子质量的1/1836 |
原子核又由两种粒子构成:
| 构成部分 | 电性 | 相对质量(约) |
|---|---|---|
| 质子 | 带正电 (+) | 1 |
| 中子 | 不带电 (中性) | 1 |
核电荷数、质子数、核外电子数的关系
这是最重要的一个关系式,必须牢记:
核电荷数 = 质子数 = 核外电子数

(图片来源网络,侵删)
- 核电荷数:原子核所带的电荷数,等于质子数。
- 原子:不显电性,因为质子数(+)和核外电子数(-)相等,电量相互抵消。
- 离子:原子得失电子后形成的带电粒子。
- 阳离子:原子失去电子后,核外电子数 < 质子数,带正电。 (如:Na⁺, Ca²⁺)
- 阴离子:原子得到电子后,核外电子数 > 质子数,带负电。 (如:Cl⁻, O²⁻)
相对原子质量
- 定义:以一种碳原子质量的1/12作为标准,其他原子的质量与它相比较所得到的比。
- 计算公式:相对原子质量 ≈ 质子数 + 中子数
- 注意:相对原子质量是一个比值,单位为“1”,通常省略不写。
第二部分:元素
元素的概念
- 定义:质子数(即核电荷数)相同的一类原子的总称。
- 质子数相同,这是判断是否为同种元素的唯一标准。
- 举例:
- 氢原子、氢离子(H⁺)的质子数都是1,它们都属于氢元素。
- 氧原子、氧离子(O²⁻)的质子数都是8,它们都属于氧元素。
元素与原子的区别与联系
| 项目 | 元素 | 原子 |
|---|---|---|
| 定义 | 质子数相同的一类原子的总称 | 化学变化中的最小微粒 |
| 特征 | 宏观概念,只讲种类,不讲个数 | 微观概念,既讲种类,也讲个数 |
| 使用范围 | 描述物质的宏观组成 (如:水是由氢元素和氧元素组成的) | 描述物质的微观构成 (如:一个水分子是由两个氢原子和一个氧原子构成的) |
| 联系 | 元素是同类原子的总称,原子是元素的最小粒子 |
元素符号
- 意义:
- 宏观:表示一种元素。(H表示氢元素)
- 微观:表示该元素的一个原子。(H表示一个氢原子)
- 特例:对于由原子直接构成的物质,元素符号还表示这种物质本身。
Fe(铁)可以表示:①铁元素;②一个铁原子;③铁这种物质。
- 书写:
- 由一个字母表示:大写。(H, O, C)
- 由两个字母表示:第一个大写,第二个小写。(Na, Ca, Cu)
元素周期表简介
- 结构:周期表按原子序数递增的顺序排列。
- 周期:横行,共7个周期,同一周期原子的电子层数相同。
- 族:纵行,共18个族,同一族原子的最外层电子数相同,化学性质相似。
- 原子序数:按元素在周期表中原子核电荷数递增的顺序给元素的编号。 原子序数 = 质子数 = 核电荷数 = 核外电子数
第三部分:离子
核外电子的排布
- 分层排布:核外电子在能量不同的电子层上运动,能量低的离核近,能量高的离核远。
- 排布规律:
- 分层:电子层由内向外依次为 K, L, M, N... (或 1, 2, 3, 4...)
- 最外层不超过8个电子(第一层不超过2个)。
- 次外层不超过18个电子。
- 结构示意图:圆圈表示原子核及核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
离子的形成
- 目的:原子通过得失电子,使最外层达到相对稳定结构(通常为8个电子,第一层为2个)。
- 过程:
- 金属元素(如Na, Mg):最外层电子数较少(<4),容易失去电子,形成阳离子。
- 非金属元素(如Cl, O):最外层电子数较多(≥4),容易得到电子,形成阴离子。
- 表示方法:在元素符号右上角标出电荷数和电性。
Na⁺ (带1个单位正电荷),Cl⁻ (带1个单位负电荷),Mg²⁺ (带2个单位正电荷),O²⁻ (带2个单位负电荷)。
第四部分:化学式与化合价
化学式
- 定义:用元素符号和数字的组合表示物质组成的式子。
- 意义:
- 宏观:表示一种物质;表示该物质由哪些元素组成。 (H₂O表示水;表示水由氢元素和氧元素组成)
- 微观:表示该物质的一个分子;表示一个分子由哪些原子构成。 (H₂O表示一个水分子;表示一个水分子由2个氢原子和1个氧原子构成)
- 写法与读法:
- 单质化学式:直接用元素符号表示(如:He, Fe, O₂)。
- 化合物化学式:正价元素在前,负价元素在后(NH₃等除外),原子个数写在右下角。
- 读法:从右到左,读作“某化某”,如 NaCl 读作氯化钠,若含原子团,读作“某酸某”或“氢某化某”。
化合价
- 定义:元素在形成化合物时表现出的一种性质。
- 规则:
- 化合物中,正负化合价代数和为零。
- 单质中,元素化合价为零。
- 在化合物中,通常氧显-2价,氢显+1价。
- 金属元素通常显正价,非金属元素通常显负价(但非金属与氧结合时显正价)。
- 应用:
- 检验化学式的正误。
- 根据化合价书写化学式(十字交叉法)。
- 口诀:排序标价,交叉约简,原子个数,写在右下。
- 根据化学式计算某元素的化合价。
重点与难点总结
-
重点:
- 原子的构成(质子、中子、电子的关系)。
- 元素的概念(质子数决定元素种类)。
- 元素符号的意义。
- 离子的形成过程。
- 化学式的意义。
- 化合价的应用(书写化学式、计算化合价)。
-
难点:
 (图片来源网络,侵删)
(图片来源网络,侵删)- 宏观与微观的对应关系:能准确区分“物质由元素组成”和“分子由原子构成”这两种说法。
- 相对原子质量的计算:理解“≈”的含义,知道为什么可以这样算。
- 离子化合物与共价化合物的初步理解(九年级要求不高,但要知道离子是通过得失电子形成的)。
- 化合价的应用:特别是利用化合价规则来书写和判断化学式,是易错点。
学习方法建议
- 构建知识网络:用思维导图将“原子-元素-离子-化学式-化合价”这些概念串联起来,理清它们之间的逻辑关系。
- 理解记忆:不要死记硬背,理解了原子得失电子是为了达到稳定结构,就很容易记住离子的形成过程。
- 多做练习:特别是关于化学式书写和化合价计算的题目,通过反复练习来巩固。
- 归纳总结:常见元素和原子团的化合价最好能背下来,可以编成口诀(如:钾钠银氢正一价,钙镁钡锌正二价...)。
- 联系实际:思考生活中常见的物质(如水、食盐、氧气)的组成和构成,用学到的微观知识去解释宏观现象。
希望这份详细的梳理能帮助你更好地学习第四单元!祝你学习进步!