九年级化学上册第三单元核心知识有哪些?
校园之窗 2025年12月19日 21:02:59 99ANYc3cd6
单元核心脉络
本单元可以大致分为三个核心板块:
- 物质由微观粒子构成:认识构成物质的基本微粒——分子、原子。
- 原子的构成:深入到原子内部,探索原子的结构。
- 元素与元素周期表:将微观的原子与宏观的物质分类联系起来,建立元素的概念。
第一部分:分子和原子
这是本单元的入门,也是整个微观理论的起点。
(图片来源网络,侵删)
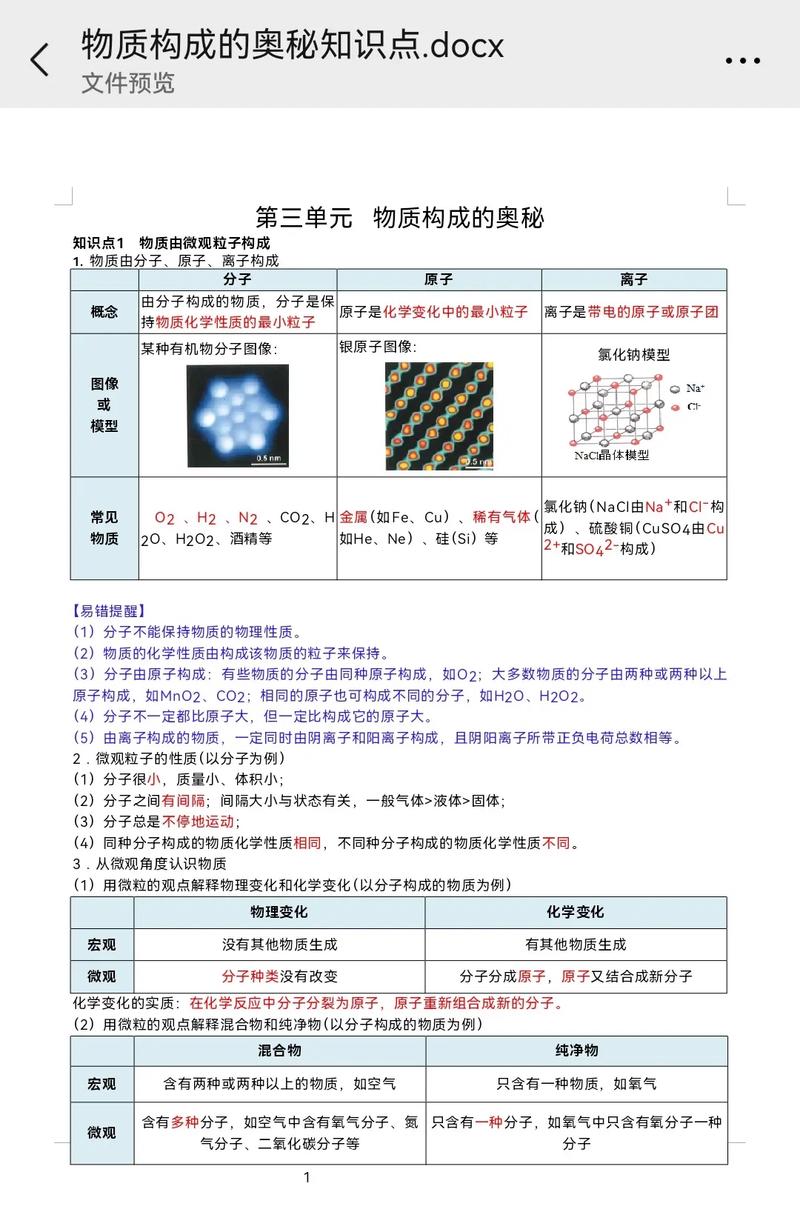
物质由微观粒子构成
- 核心观点:物质是由分子、原子等微观粒子构成的。
- 由分子构成的物质:许多物质(如水 H₂O、氧气 O₂、二氧化碳 CO₂、酒精 C₂H₅OH)是由分子构成的,分子是保持物质化学性质的最小粒子。
- 由原子构成的物质:少数物质(如金属、稀有气体、金刚石、石墨等)是由原子直接构成的,原子是化学变化中的最小粒子。
分子的基本性质
这是理解分子概念的关键,也是解释宏观现象的微观依据。
- 质量和体积都很小。
- 分子在不停地做无规则运动。
- 微观解释:闻到花香、湿衣服晾干、糖溶于水、品红扩散等现象,都是分子运动的结果。
- 影响因素:温度越高,分子运动越剧烈。
- 分子之间有间隔。
- 微观解释:物质的热胀冷缩、三态变化(固、液、气)、物质混合后总体积小于原体积之和(如50ml水+50ml酒精<100ml)等现象,都是分子间隔改变的结果。
- 三态中分子间隔大小:气体 > 液体 > 固体。
- 同种物质的分子性质相同,不同种物质的分子性质不同。
原子
- 定义:原子是化学变化中的最小粒子。
- 理解“最小”:在化学变化中,分子可以再分,而原子不能再分,原子在化学变化中只是重新组合,没有变成其他原子。
- 联系:分子是由原子构成的,一个水分子(H₂O)是由2个氢原子和1个氧原子构成的。
分子与原子的区别和联系
| 分子 | 原子 | |
|---|---|---|
| 定义 | 保持物质化学性质的最小粒子 | 化学变化中的最小粒子 |
| 在化学变化中 | 可以再分,变成其他原子 | 不可再分 |
| 构成 | 由原子构成 | 由更小的微粒(质子、中子、电子)构成 |
| 本质联系 | 分子是由原子构成的,分子是构成物质的一种微粒,原子是构成分子的微粒,也是直接构成物质的微粒。 |
第二部分:原子的构成
这部分深入到原子内部,揭示了原子的奥秘。
原子的结构模型(卢瑟福行星模型)
- 构成:原子由原子核和核外电子构成。
- 原子核:位于原子中心,体积很小,但集中了原子的几乎全部质量。
- 核外电子:在原子核外做高速运动。
- 类比:就像太阳系,原子核是太阳,电子是绕着太阳转的行星。
构成原子的三种粒子
| 粒子 | 电性 | 质量 | 作用 |
|---|---|---|---|
| 质子 | 带1个单位正电荷 | 相对质量约为1 | 决定元素的种类 |
| 中子 | 不带电(电中性) | 相对质量约为1 | 决定原子的质量,影响同位素 |
| 电子 | 带1个单位负电荷 | 质量很小,约为质子质量的1/1836 | 决定元素的化学性质 |
核电荷数、质子数、核外电子数的关系
-
在原子中:
- 核电荷数 = 质子数(因为原子核带正电,其电荷数由质子数决定)
- 质子数 = 核外电子数(原子不显电性,所以正电荷总数与负电荷总数相等)
- 原子序数 = 质子数 = 核电荷数 = 核外电子数
-
在离子中:
 (图片来源网络,侵删)
(图片来源网络,侵删)- 阳离子:原子失去电子后带正电,质子数 > 核外电子数。
- 阴离子:原子得到电子后带负电,质子数 < 核外电子数。
相对原子质量
- 定义:以一种碳原子质量的 1/12 作为标准,其他原子的质量与它相比较所得到的比,作为这种原子的相对原子质量(符号为 Ar)。
- 近似计算:相对原子质量 ≈ 质子数 + 中子数(因为电子质量太小,可以忽略不计)。
第三部分:元素与元素周期表
这是连接微观世界和宏观世界的桥梁。
元素
- 定义:质子数(即核电荷数)相同的一类原子的总称。
- 质子数相同,这是判断是否为同种元素的根本依据。
- 理解:
- 元素是宏观概念,只讲种类,不讲个数,不能说“一个氧元素”,只能说“氧元素”。
- 原子是微观概念,既讲种类,也讲个数,可以说“一个氧原子”。
- 关系:元素是原子的归类,所有质子数为1的原子(氢原子、氕、氘、氚)统称为氢元素。
- 元素的分类:
- 金属元素:如铁、铜、钠、钙(汉字一般带“钅”旁,汞除外)。
- 非金属元素:如碳、氧、氢、硫(汉字一般带“石”、“气”、“氵”旁等)。
- 稀有气体元素:如氦、氖、氩(化学性质非常稳定)。
元素符号
- 意义:
- 宏观:表示一种元素,H 表示氢元素。
- 微观:表示该元素的一个原子,H 表示一个氢原子。
- 注意事项:
- 当符号前有数字时,只表示微观意义(几个原子),2H 只表示“两个氢原子”,不表示“氢元素”。
- 由原子构成的物质,元素符号还可表示这种物质,Fe 表示铁元素、一个铁原子,也表示铁这种物质。
元素周期表简介
- 结构:周期表按原子序数(质子数)递增的顺序给元素编号。
- 横行——周期:共有7个周期,每一周期元素的原子核外电子层数相同。
- 纵列——族:共有18个族,同一族元素的化学性质相似。
- 单元格信息:以氧元素为例
- 原子序数:8(即质子数=8)
- 元素符号:O
- 元素名称:氧
- 相对原子质量:约 16.00 (取整数约为16)
本单元重点与难点总结
-
重点:
- 分子的基本性质及其应用(解释现象)。
- 分子和原子的区别与联系。
- 原子的构成(质子、中子、电子的关系)。
- 元素的概念(质子数相同)。
- 元素符号的意义。
-
难点:
- 建立微观粒子观:从看得见、摸得着的宏观世界,过渡到看不见、摸不着的微观世界,需要较强的抽象思维能力。
- 区分“分子”、“原子”、“元素”:这三个概念是易混点,必须从宏观/微观、种类/个数等角度清晰区分。
- 理解“化学变化中的最小粒子”:原子在化学变化中“不可再分”是相对的,在核反应中可以再分,但在初中化学范畴内,这个定义是成立的。
- 离子与原子的转化:理解原子得失电子变成离子的过程。
学习方法建议
- 多画图:画出分子运动示意图、原子结构示意图、元素周期表结构图,将抽象概念形象化。
- 多对比:制作表格对比分子与原子、原子与离子、元素与原子的异同。
- 多联系实际:用分子原子的理论去解释生活中的现象,如为什么气体容易被压缩,为什么墙内开花墙外香等。
- 记忆口诀:可以编一些简单的口诀帮助记忆,如“分子小,运动快,有间隔,同种性质同种类”。
希望这份详细的梳理能帮助你更好地理解和掌握九年级化学上册第三单元的知识!










