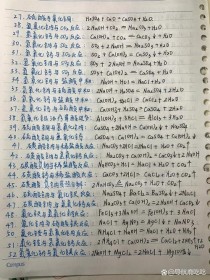
九年级化学上册方程式有哪些?
校园之窗 2026年1月29日 21:40:58 99ANYc3cd6
化学方程式的基础
在记忆方程式之前,请务必理解以下几点:
- 书写原则:
- 以客观事实为基础:不能臆造不存在的物质或反应。
- 遵守质量守恒定律:方程式必须配平,即反应前后各原子的种类和数目相等。
- 书写步骤:“写 → 配 → 等 → 注”
- 写:写出反应物和生成物的化学式。
- 配:在化学式前配上适当的化学计量数,使反应前后各原子数目相等。
- 等:将短线改为等号。
- 注:注明反应条件(如点燃、加热、催化剂等)和生成物的状态(气体↑,沉淀↓)。
- 常见反应条件:
点燃(或 ): 加热高温: 较高温度加热通电: 通入直流电催化剂: 如MnO₂
按基本反应类型分类
这是最核心的分类方法,有助于理解反应的本质。

(图片来源网络,侵删)
化合反应 (多变一)
-
(1) 与氧气的反应 (燃烧/氧化)
- 镁条燃烧:发出耀眼白光,生成白色固体。
2Mg + O₂ --(点燃)--> 2MgO - 铁丝在氧气中燃烧:剧烈燃烧,火星四射,生成黑色固体。
3Fe + 2O₂ --(点燃)--> Fe₃O₄ - 铜丝在空气中加热:铜表面变黑。
2Cu + O₂ --(△)--> 2CuO - 红磷燃烧:产生大量白烟。
4P + 5O₂ --(点燃)--> 2P₂O₅ - 硫磺燃烧:在空气中淡蓝色火焰,在氧气中蓝紫色火焰,产生有刺激性气味的气体。
S + O₂ --(点燃)--> SO₂ - 氢气燃烧:纯净的氢气在空气中安静燃烧,产生淡蓝色火焰。
2H₂ + O₂ --(点燃)--> 2H₂O - 一氧化碳燃烧:产生蓝色火焰。
2CO + O₂ --(点燃)--> 2CO₂ - 碳充分燃烧:发出白光。
C + O₂ --(点燃)--> CO₂ - 碳不充分燃烧:
2C + O₂ --(点燃)--> 2CO
- 镁条燃烧:发出耀眼白光,生成白色固体。
-
(2) 其他化合反应
- 二氧化碳和水反应:生成碳酸,使紫色石蕊试液变红。
CO₂ + H₂O == H₂CO₃ - 生石灰与水反应:放出大量热,生成熟石灰(重要放热反应)。
CaO + H₂O == Ca(OH)₂ - 一氧化碳还原氧化铜:虽然常归为还原反应,但也是化合反应的逆反应。
CO + CuO --(△)--> Cu + CO₂
- 二氧化碳和水反应:生成碳酸,使紫色石蕊试液变红。
分解反应 (一变多)
-
(1) 实验室制取氧气
- 过氧化氢溶液制氧气:二氧化锰作催化剂。
2H₂O₂ --(MnO₂)--> 2H₂O + O₂↑ - 高锰酸钾制氧气:加热。
2KMnO₄ --(△)--> K₂MnO₄ + MnO₂ + O₂↑ - 氯酸钾制氧气:二氧化锰作催化剂,加热。
2KClO₃ --(MnO₂, △)--> 2KCl + 3O₂↑
- 过氧化氢溶液制氧气:二氧化锰作催化剂。
-
(2) 电解水
 (图片来源网络,侵删)
(图片来源网络,侵删)- 正极产生氧气,负极产生氢气,体积比约为1:2。
2H₂O --(通电)--> 2H₂↑ + O₂↑
- 正极产生氧气,负极产生氢气,体积比约为1:2。
-
(3) 其他分解反应
- 加热碳酸氢铵:生成氨气、水和二氧化碳。
NH₄HCO₃ --(△)--> NH₃↑ + H₂O + CO₂↑ - 煅烧石灰石:工业上制取二氧化碳和生石灰。
CaCO₃ --(高温)--> CaO + CO₂↑ - 加热氧化汞:
2HgO --(△)--> 2Hg + O₂↑
- 加热碳酸氢铵:生成氨气、水和二氧化碳。
置换反应 (一换一)
-
(1) 金属与酸反应
- 锌与稀硫酸:实验室制氢气的常用方法。
Zn + H₂SO₄ == ZnSO₄ + H₂↑ - 铁与稀硫酸:溶液由无色变为浅绿色。
Fe + H₂SO₄ == FeSO₄ + H₂↑ - 镁与稀盐酸:反应速率快,放出大量热。
Mg + 2HCl == MgCl₂ + H₂↑ - 铝与稀盐酸:
2Al + 6HCl == 2AlCl₃ + 3H₂↑ - 铜与稀盐酸/稀硫酸:不反应(因为铜排在氢后)。
- 锌与稀硫酸:实验室制氢气的常用方法。
-
(2) 金属与盐溶液反应
- 铁与硫酸铜溶液:湿法炼铜,铁表面附着一层红色物质,溶液由蓝色变为浅绿色。
Fe + CuSO₄ == FeSO₄ + Cu - 锌与硫酸铜溶液:
Zn + CuSO₄ == ZnSO₄ + Cu - 铜与硝酸银溶液:铜表面附着一层银白色物质,溶液由无色变为蓝色。
Cu + 2AgNO₃ == Cu(NO₃)₂ + 2Ag - 铝与硫酸铜溶液:
2Al + 3CuSO₄ == Al₂(SO₄)₃ + 3Cu
- 铁与硫酸铜溶液:湿法炼铜,铁表面附着一层红色物质,溶液由蓝色变为浅绿色。
-
(3) 其他置换反应
- 碳还原氧化铜:黑色粉末变红色,生成使澄清石灰水变浑浊的气体。
C + 2CuO --(高温)--> 2Cu + CO₂↑ - 氢气还原氧化铜:黑色粉末变红色,试管口有水珠生成。
H₂ + CuO --(△)--> Cu + H₂O
- 碳还原氧化铜:黑色粉末变红色,生成使澄清石灰水变浑浊的气体。
复分解反应 (交换成分)
-
(1) 中和反应 (酸 + 碱 → 盐 + 水)
- 氢氧化钠与盐酸:
NaOH + HCl == NaCl + H₂O - 氢氧化钙与盐酸:
Ca(OH)₂ + 2HCl == CaCl₂ + 2H₂O - 氢氧化铝与盐酸:治疗胃酸过多。
Al(OH)₃ + 3HCl == AlCl₃ + 3H₂O
- 氢氧化钠与盐酸:
-
(2) 酸 + 盐 → 新酸 + 新盐
- 大理石/石灰石与稀盐酸:实验室制取二氧化碳。
CaCO₃ + 2HCl == CaCl₂ + H₂O + CO₂↑ - 碳酸钠与稀盐酸:反应剧烈,生成大量气泡。
Na₂CO₃ + 2HCl == 2NaCl + H₂O + CO₂↑ - 硝酸银与稀盐酸:生成不溶于稀硝酸的白色沉淀(检验Cl⁻)。
AgNO₃ + HCl == AgCl↓ + HNO₃
- 大理石/石灰石与稀盐酸:实验室制取二氧化碳。
-
(3) 碱 + 盐 → 新碱 + 新盐
- 氢氧化钠与硫酸铜溶液:生成蓝色沉淀。
2NaOH + CuSO₄ == Cu(OH)₂↓ + Na₂SO₄ - 氢氧化钠与氯化铁溶液:生成红褐色沉淀。
3NaOH + FeCl₃ == Fe(OH)₃↓ + 3NaCl - 氢氧化钙与碳酸钠溶液:生成白色沉淀。
Ca(OH)₂ + Na₂CO₃ == CaCO₃↓ + 2NaOH
- 氢氧化钠与硫酸铜溶液:生成蓝色沉淀。
-
(4) 盐 + 盐 → 两种新盐
- 氯化钡与硫酸钠溶液:生成不溶于稀硝酸的白色沉淀(检验SO₄²⁻)。
BaCl₂ + Na₂SO₄ == BaSO₄↓ + 2NaCl - 硝酸银与氯化钠溶液:
AgNO₃ + NaCl == AgCl↓ + NaNO₃
- 氯化钡与硫酸钠溶液:生成不溶于稀硝酸的白色沉淀(检验SO₄²⁻)。
按核心实验/主题分类
实验室制取气体
- 制取氧气 (O₂)
2H₂O₂ --(MnO₂)--> 2H₂O + O₂↑2KMnO₄ --(△)--> K₂MnO₄ + MnO₂ + O₂↑
- 制取氢气 (H₂)
Zn + H₂SO₄ == ZnSO₄ + H₂↑
- 制取二氧化碳 (CO₂)
CaCO₃ + 2HCl == CaCl₂ + H₂O + CO₂↑
燃烧与灭火
- 燃烧的三个条件:可燃物、氧气(或空气)、达到着火点。
- 灭火的原理:破坏任意一个燃烧条件(清除可燃物、隔绝氧气、降温至着火点以下)。
- 相关方程式:主要看与氧气的化合反应(见上文)。
碳和碳的氧化物
- 碳的化学性质
C + O₂ --(点燃)--> CO₂(充分燃烧)2C + O₂ --(点燃)--> 2CO(不充分燃烧)C + 2CuO --(高温)--> 2Cu + CO₂↑(还原性)
- 一氧化碳的化学性质
2CO + O₂ --(点燃)--> 2CO₂(可燃性)CO + CuO --(△)--> Cu + CO₂(还原性)
- 二氧化碳的化学性质
CO₂ + H₂O == H₂CO₃(酸性氧化物)CO₂ + Ca(OH)₂ == CaCO₃↓ + H₂O(检验CO₂)CaCO₃ --(高温)--> CaO + CO₂↑(工业制CO₂)
金属及其化合物
- 金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
- 排在前面的金属能把排在后面的金属从它们的盐溶液中置换出来。
- 排在氢前面的金属能置换出酸中的氢。
- 铁的锈蚀与防护
- 锈蚀条件:铁与氧气、水同时接触。
- 防锈原理:隔绝氧气或水。
- 除铁锈:用稀盐酸或稀硫酸。
Fe₂O₃ + 6HCl == 2FeCl₃ + 3H₂O
记忆方法与技巧
- 理解记忆:不要死记硬背,理解每个反应的原理、现象和实验目的,记忆会更深刻。
- 分类记忆:按照上面的分类法,将零散的方程式系统化,形成知识网络。
- 实验联想:把方程式和具体的实验现象(如颜色变化、气体生成、沉淀产生、放热发光等)联系起来,看到方程式,就能在脑海中“播放”实验视频。
- 口诀记忆:
- 化合反应口诀:
氧镁白,铁四氧,铜黑磷五氧,硫二氧氢二氧,碳充分生二氧,不充分生一氧。 - 实验室制氧气口诀:
一氯二锰高锰酸。(指氯酸钾、过氧化氢、高锰酸钾) - 金属活动性顺序口诀:
钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。
- 化合反应口诀:
- 多写多用:亲手书写,反复练习,在做题和实验中不断应用,才能真正掌握。
希望这份详细的总结对你有帮助!祝你学习进步!