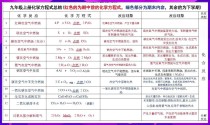
9年级下册化学核心知识点有哪些?
校园之窗 2026年1月29日 11:39:24 99ANYc3cd6
九年级下册化学核心知识体系
九年级下册的化学主要围绕 “酸、碱、盐” 这三大类物质展开,并在此基础上学习化学与生活、化学与材料的联系,其核心逻辑是:
- 认识物质:酸、碱、盐的定义、通性和化学性质。
- 理解反应:酸、碱、盐之间的复分解反应及其发生条件。
- 应用原理:酸碱中和反应、溶液的酸碱度(pH)及其应用。
- 拓展视野:化学肥料、常见的材料(金属、有机合成材料)。
第一单元:酸和碱
酸和碱的通性
这是本册书的重中之重,需要对比记忆。

(图片来源网络,侵删)
| 类别 | 酸 | 碱 |
|---|---|---|
| 定义 | 电离时产生的阳离子全部是氢离子(H⁺)的化合物。 | 电离时产生的阴离子全部是氢氧根离子(OH⁻)的化合物。 |
| 溶液的pH | pH < 7 (pH越小,酸性越强) | pH > 7 (pH越大,碱性越强) |
| 指示剂变色 | 紫色石蕊试液:变红 无色酚酞试液:不变色 (仍为无色) |
紫色石蕊试液:变蓝 无色酚酞试液:变红 |
| 通性1 (与指示剂) | 使紫色石蕊变红,酚酞不变色 | 使紫色石蕊变蓝,酚酞变红 |
| 通性2 (与活泼金属) | + 金属 → 盐 + 氢气 (H₂) 例: Zn + H₂SO₄ = ZnSO₄ + H₂↑ |
- |
| 通性3 (与金属氧化物) | + 金属氧化物 → 盐 + 水 例: CuO + 2HCl = CuCl₂ + H₂O |
+ 非金属氧化物 → 盐 + 水 例: 2NaOH + CO₂ = Na₂CO₃ + H₂O |
| 通性4 (与碱) | + 碱 → 盐 + 水 (中和反应) | + 酸 → 盐 + 水 (中和反应) |
| 通性5 (与某些盐) | + 盐 → 新盐 + 新酸 例: AgNO₃ + HCl = AgCl↓ + HNO₃ |
+ 盐 → 新盐 + 新碱 例: CuSO₄ + 2NaOH = Cu(OH)₂↓ + Na₂SO₄ |
| 常见例子 | 盐酸(HCl)、硫酸(H₂SO₄)、硝酸(HNO₃) | 氢氧化钠、氢氧化钙、氢氧化钾 |
【核心记忆点】
- 酸的“个性”:
- 盐酸:有刺激性气味,挥发性,浓盐酸在空气中会形成“白雾”(挥发出的HCl气体与水蒸气结合)。
- 硫酸:吸水性(作干燥剂),浓硫酸具有强烈的腐蚀性,稀释时必须将浓硫酸沿器壁慢慢注入水中,并不断搅拌(酸入水,沿壁,勤搅拌)。
- 碱的“个性”:
- 氢氧化钠:俗称烧碱、火碱、苛性钠,易潮解(作干燥剂),有强烈的腐蚀性,必须密封保存。
- 氢氧化钙:俗称熟石灰、消石灰,微溶于水,其水溶液俗称石灰水,可由生石灰(CaO)与水反应制得:
CaO + H₂O = Ca(OH)₂(此反应放热)。
第二单元:盐和化肥
常见的盐
| 名称 | 化学式 | 俗称 / 主要性质 / 用途 |
|---|---|---|
| 氯化钠 | NaCl | 食盐,生活调味品、生理盐水、融雪剂。 |
| 碳酸钠 | Na₂CO₃ | 纯碱、苏打(不是碱,是盐),水溶液呈碱性,用于玻璃、造纸、洗涤剂。 |
| 碳酸氢钠 | NaHCO₃ | 小苏打,受热易分解:2NaHCO₃ --(加热)--> Na₂CO₃ + H₂O + CO₂↑,用于发酵粉、治疗胃酸过多。 |
| 碳酸钙 | CaCO₃ | 大理石、石灰石、蛋壳、贝壳的主要成分,难溶于水,高温分解:CaCO₃ --(高温)--> CaO + CO₂↑,用作建筑材料、补钙剂。 |
粗盐提纯
步骤:溶解 → 过滤 → 蒸发
- 溶解:用玻璃棒搅拌,加速溶解。
- 过滤:“一贴、二低、三靠”。
- 一贴:滤纸紧贴漏斗内壁。
- 二低:滤纸边缘低于漏斗边缘;液面低于滤纸边缘。
- 三靠:烧杯口紧靠玻璃棒;玻璃棒末端轻靠三层滤纸一侧;漏斗末端紧靠烧杯内壁。
- 蒸发:用玻璃棒不断搅拌,防止局部温度过高造成液滴飞溅,当出现较多固体时停止加热。
复分解反应
这是本册书的另一个核心和难点。
-
定义:由两种化合物相互交换成分,生成另外两种新化合物的反应。
 (图片来源网络,侵删)
(图片来源网络,侵删)- 通式:AB + CD → AD + CB
-
发生条件(必须满足至少一个):
- 生成沉淀 (如 BaSO₄, CaCO₃, AgCl 等)
- 生成气体 (如 CO₂, NH₃ 等)
- 生成水 (H₂O)
【判断方法】
- 看产物:反应物交换成分后,看生成的物中是否有沉淀、气体或水。
- 记口诀:钾盐、钠盐、铵盐、硝酸盐,全都溶;盐酸盐(氯化物)不溶银亚汞;硫酸盐不溶钡和铅;碳酸盐、磷酸盐只溶钾钠铵。
【典型反应】
- 酸 + 碱 → 盐 + 水 (中和反应,一定发生)
- 酸 + 盐 → 新盐 + 新酸 (如
HCl + AgNO₃ = AgCl↓ + HNO₃) - 碱 + 盐 → 新碱 + 新盐 (如
2NaOH + CuSO₄ = Cu(OH)₂↓ + Na₂SO₄) - 盐 + 盐 → 两种新盐 (如
BaCl₂ + Na₂SO₄ = BaSO₄↓ + 2NaCl)
第三单元:酸和碱的反应(深化)
中和反应
- 定义:酸与碱作用生成盐和水的反应。
- 实质:酸溶液中的 H⁺ 和碱溶液中的 OH⁻ 结合生成了水分子 (H₂O)。
- 应用:
- 改变土壤的酸碱性:如用熟石灰改良酸性土壤。
- 处理工厂废水:如用熟石灰处理含硫酸的废水。
- 医药应用:如用含氢氧化铝的药物治疗胃酸过多。
- 调节食品的酸碱度。
溶液的酸碱度——pH
- pH范围:0 ~ 14
- pH = 7,溶液呈中性。
- pH < 7,溶液呈酸性,pH越小,酸性越强。
- pH > 7,溶液呈碱性,pH越大,碱性越强。
- pH的测定:用pH试纸。
- 方法:在玻璃片上放一片pH试纸,用玻璃棒蘸取待测液滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,读出pH值。
- 注意:不能将pH试纸直接伸入待测液中,也不能将试纸润湿。
- pH的应用:
- 农业:了解土壤的pH,选择合适的作物或进行改良。
- 工业:控制反应条件。
- 生活:洗发水(弱酸性)和护发素(弱碱性)搭配使用。
第四单元:化学与生活
化学肥料
化肥主要提供氮、磷、钾三种营养元素。

(图片来源网络,侵删)
| 类型 | 作用 | 常见例子 | 缺乏症状 |
|---|---|---|---|
| 氮肥 | 促进植物茎、叶生长茂盛,叶色浓绿 | 尿素[CO(NH₂)₂]、氨水(NH₃·H₂O)、铵盐 | 植物矮小,叶片发黄 |
| 磷肥 | 促进植物根系发达,增强抗寒抗旱能力 | 磷矿粉[Ca₃(PO₄)₂]、钙镁磷肥 | 植物生长迟缓,果实籽粒不饱满 |
| 钾肥 | 促进植物茎秆粗壮,增强抗病虫害和倒伏能力 | 硫酸钾(K₂SO₄)、氯化钾 | 植物茎秆软弱,易倒伏 |
| 复合肥 | 同时含有两种或两种以上营养元素 | 硝酸钾(KNO₃)、磷酸二氢铵(NH₄H₂PO₄) | - |
常见的材料
-
金属材料:
- 合金:在金属中加热熔合某些金属或非金属,得到的具有金属特性的物质,合金的性能一般优于纯金属。
- 常见合金:铁合金(生铁、钢)、黄铜(铜锌合金)、铝合金等。
-
无机非金属材料:
- 水泥、玻璃、陶瓷是三大传统无机非金属材料。
-
有机合成材料:
- 三大合成材料:塑料、合成纤维、合成橡胶。
- 鉴别方法:
- 燃烧法:燃烧时有特殊气味,燃烧后结焦的是羊毛、棉花(天然纤维);燃烧无焦味,熔化成滴状的是合成纤维。
- “白色污染”:指废弃塑料对环境的污染,解决方法:减少使用、重复使用、使用可降解塑料、回收利用。
第五单元:化学计算(下册重点)
九年级下册的计算主要围绕溶液展开。
溶液的相关概念
- 溶液:一种或几种物质分散到另一种物质中,形成的均一、稳定的混合物。
- 溶质:被溶解的物质。
- 溶剂:能溶解其他物质的物质,水是最常见的溶剂。
- 饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能再继续溶解时,所得到的溶液。
- 不饱和溶液:还能继续溶解某种溶质的溶液。
- 浓溶液与稀溶液:指溶质含量的多少,与是否饱和无关。
溶液中溶质的质量分数 (ω)
- 定义:溶质的质量与溶液的质量之比。
- 公式:
ω(溶质的质量分数) = (溶质的质量 / 溶液的质量) × 100%溶液的质量 = 溶质的质量 + 溶剂的质量 - 常见计算类型:
- 基本计算:已知溶质和溶液质量,求质量分数。
- 溶液稀释:稀释前后,溶质的质量不变。
浓溶液质量 × 浓溶液质量分数 = 稀溶液质量 × 稀溶液质量分数 - 涉及化学反应的计算:根据化学方程式计算反应后生成物的质量,再求溶质的质量分数。注意:溶液的质量不一定是反应物质量之和,要考虑气体或沉淀的生成。
总结与建议
- 构建知识网络:不要孤立地记知识点,要把酸、碱、盐的性质、反应规律、用途串联起来,形成一张“关系网”。
- 重视化学方程式:化学是“理科中的文科”,化学方程式是化学的“语言”,要理解每个方程式的反应原理,并熟练书写。
- 多做归纳对比:特别是酸和碱的通性、盐的溶解性等,用表格法对比记忆,效果显著。
- 联系生活实际:思考为什么可以用醋除去水垢?为什么可以用熟石灰改良酸性土壤?理论联系实际,学起来更有趣,也记得更牢。
- 勤于练习:计算题和推断题是中考的重头戏,一定要通过大量练习来巩固解题方法和思路。
希望这份详细的梳理对你有帮助!祝你学习进步,中考取得优异成绩!