元素周期表怎么记?八年级化学重点难点?
校园之窗 2026年1月22日 08:53:00 99ANYc3cd6
第一部分:什么是元素周期表?
你可以把元素周期表想象成一张“化学家的大地图”或“元素的身份证”。
- 地图:它把世界上已经发现的100多种元素(截至2025年共118种)按照一定的规律排列起来,就像地图把城市和地区排列起来一样,通过这张地图,我们可以知道每个元素的基本信息,以及它们之间的关系。
- 身份证:每一格代表一个元素,上面有这个元素的“姓名”(中文名、元素符号)、“住址”(原子序数)和“性格”(最外层电子数等)。
第二部分:看懂元素周期表的“身份证”——一格代表什么
我们先来看一张元素周期表的一部分,以我们最熟悉的氢和氦为例:
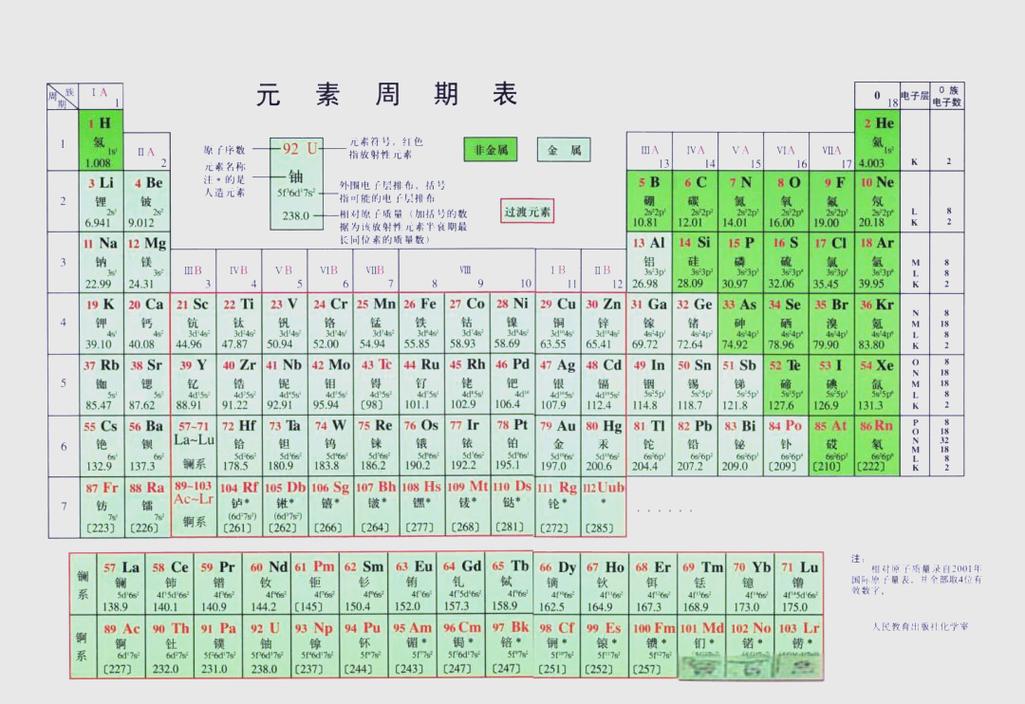
(图片来源网络,侵删)
| 1 H 氢 1.008 |
2 He 氦 4.003 |
|||||||||||||||||
| 3 Li 锂 6.94 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|||||||||||
| ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... | ... |
解读每一格信息(以氢H为例):
-
原子序数:位于格子的左上角。
- 含义:代表该元素原子核中的质子数,在原子中,质子数=核外电子数。
- 特点:这是元素的“身份证号”,一个原子序数对应一种特定的元素,独一无二。
- 氢的原子序数是1,说明它的原子核里有1个质子,核外也有1个电子。
-
元素符号:位于格子的中间。
- 含义:该元素的英文缩写,国际通用。
- 规则:通常由一个或两个字母组成,第一个字母大写,第二个字母小写。
- 氢是 H,氦是 He,钠是 Na (来自拉丁文 Natrium),铜是 Cu (来自拉丁文 Cuprum)。
-
元素名称:位于格子中间的元素符号下方(中文版)。
氢、氦、锂。
-
相对原子质量:位于格子的下方。
- 含义:该元素一个原子的平均质量与一个碳-12原子质量的1/12的比值,简单理解,可以看作是质子和中子质量总和的近似值。
- 注意:这个数值通常在小数点后取近似值,八年级计算时可以直接使用这个近似值,氢约为1,碳约为12,氧约为16。
第三部分:元素周期表的“大地图”规律——结构
这张地图不是随便排列的,它遵循两大规律:周期(横行)和族(纵列)。
周期:横行的“楼层”
- 定义:元素周期表有7个横行,每一行称为一个周期。
- 规律:
- 从左到右:核电荷数(原子序数)依次递增。
- 电子层数:同一周期的元素,其原子的电子层数相同,周期数=电子层数。
- 第1周期(H, He)的元素原子只有1个电子层。
- 第2周期(Li, Be, B, C, N, O, F, Ne)的元素原子都有2个电子层。
- 第3周期(Na, Mg, Al, Si, P, S, Cl, Ar)的元素原子都有3个电子层。
族:纵列的“家族”
- 定义:元素周期表有18个纵列,但为了方便,通常将8-9-10三个列合称为第VIII族,其余的称为第I、II...VII族,最左边两列(IA, IIA)和最右边六列(IIIA-VIIA, 0族)是主族。
- 规律:
- 从上到下:核电荷数依次递增,电子层数也依次增加。
- 最外层电子数:同一族的元素,其原子的最外层电子数相同,这是决定元素化学性质的最关键因素!
- 第IA族(氢、锂、钠、钾...)的最外层都只有1个电子。
- 第VIIA族(氟、氯、溴、碘...)的最外层都有7个电子。
- 第0族(氦、氖、氩...)也叫稀有气体元素,最外层都是8个电子(氦是2个,但也达到了稳定结构)。
第四部分:元素周期表的“性格”分类——元素分区
根据元素的性质,我们可以把周期表分成三大区域,这就像地图上的“海洋”、“陆地”和“高原”。
金属元素
- 位置:位于周期表的左下方,包括所有IA、IIA族元素,以及中间的过渡元素。
- “性格”特点:
- 通常具有金属光泽。
- 导电性、导热性良好。
- 有延展性(可以拉成丝或压成片)。
- 最外层电子数较少(一般少于4个),在化学反应中容易失去电子。
非金属元素
- 位置:位于周期表的右上角,包括第VIIA族、第VIA族、第VA族等。
- “性格”特点:
- 没有金属光泽,通常是气体或固体(溴是唯一的液体)。
- 导电性、导热性差。
- 最外层电子数较多(一般多于4个),在化学反应中容易得到电子。
稀有气体元素
- 位置:位于周期表的最右边一列(第0族)。
- “性格”特点:
- 化学性质非常稳定,很少发生化学反应,因此也叫惰性气体。
- 原因是它们的最外层电子达到了8个电子的稳定结构(氦是2个,也是最稳定结构),不想”得到也不“想”失去电子。
- 它们都是气体。
类金属/半金属元素
- 位置:位于金属元素和非金属元素的分界线上(像硼、硅、锗、砷、碲、砹等)。
- “性格”特点:既有一些金属性质,又有一些非金属性质。
第五部分:八年级必须掌握的核心规律总结
- 原子序数 = 质子数 = 核外电子数(对于原子而言)。
- 周期数 = 电子层数。
- 主族数 = 最外层电子数(仅适用于IA, IIA, IIIA-VIIA主族)。
- 元素化学性质主要由最外层电子数决定。
- 最外层电子数少(<4):易失电子,显金属性。
- 最外层电子数多(>4):易得电子,显非金属性。
- 最外层电子数8个(He为2个):结构稳定,显惰性。
- 从左到右(同一周期):
- 核电荷数递增。
- 最外层电子数递增。
- 原子半径逐渐减小。
- 金属性逐渐减弱,非金属性逐渐增强。
- 从上到下(同一族):
- 电子层数递增。
- 核电荷数递增。
- 原子半径逐渐增大。
- 金属性逐渐增强,非金属性逐渐减弱。
学习小贴士
- 不要死记硬背:理解规律比记住所有元素重要得多。
- 动手画一画:自己画一个简化的前20个元素的周期表,并标出原子序数、元素符号和最外层电子数,会加深理解。
- 分组记忆:把同一族的元素放在一起记,比如把碱金属(IA族)钠、钾、锂放在一起比较它们的相似性。
- 联系生活:想想我们身边的物质,铁是金属,氧气是非金属,空气中的氮气也是非金属,它们在周期表中的位置是怎样的?
希望这份指南能帮你打开元素周期表的大门!化学的世界非常有趣,从这张“地图”开始探索吧!加油!










