九年级相对原子质量表有何特殊之处?
校园之窗 2026年1月28日 19:11:38 99ANYc3cd6
九年级常见元素相对原子质量表 (简化版)
为了方便记忆和计算,九年级通常会使用一个简化的相对原子质量表,数值大多取整数或最接近的整数,高考或更高级别的考试则会使用更精确的数值。
| 元素名称 | 元素符号 | 相对原子质量 (九年级常用) | 相对原子质量 (精确值) | 备注 |
|---|---|---|---|---|
| 氢 | H | 1 | 008 | |
| 氦 | He | 4 | 003 | 稀有气体 |
| 碳 | C | 12 | 01 | 有机物的核心元素 |
| 氮 | N | 14 | 01 | 空气主要成分之一 |
| 氧 | O | 16 | 00 | 空气主要成分之一 |
| 氟 | F | 19 | 00 | |
| 氖 | Ne | 20 | 18 | 稀有气体 |
| 钠 | Na | 23 | 99 | 食盐的主要成分 |
| 镁 | Mg | 24 | 31 | |
| 铝 | Al | 27 | 98 | 地壳中含量最多的金属元素 |
| 硅 | Si | 28 | 09 | |
| 磷 | P | 31 | 97 | |
| 硫 | S | 32 | 06 | |
| 氯 | Cl | 5 | 45 | 九年级特例,必须记35.5 |
| 氩 | Ar | 40 | 95 | 稀有气体 |
| 钾 | K | 39 | 10 | |
| 钙 | Ca | 40 | 08 | |
| 铁 | Fe | 56 | 85 | 最常见的金属 |
| 铜 | Cu | 64 | 55 | |
| 锌 | Zn | 65 | 38 | |
| 银 | Ag | 108 | 87 | |
| 碘 | I | 127 | 90 | 加碘盐的成分 |
| 钡 | Ba | 137 | 33 | |
| 铂 | Pt | 195 | 08 | |
| 金 | Au | 197 | 97 | |
| 汞 | Hg | 201 | 59 | 唯一在常温下呈液态的金属 |
重要说明与使用技巧
什么是相对原子质量?
相对原子质量(Ar)是以一个碳-12(¹²C)原子质量的 1/12 作为标准,其他原子的质量与它相比较所得到的比值,它是一个相对质量,没有单位,是一个比值。
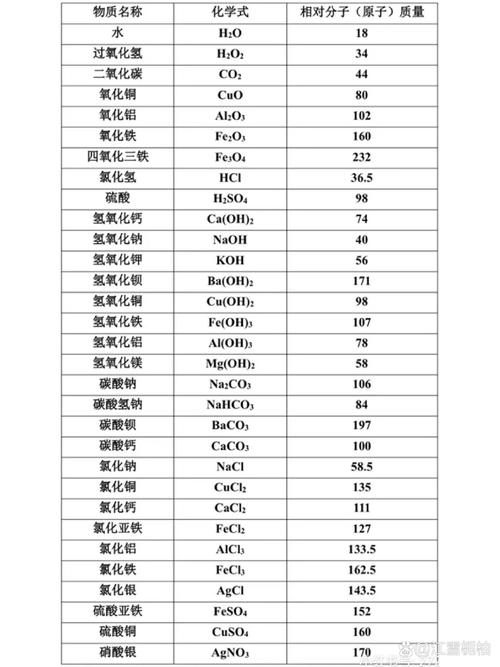
(图片来源网络,侵删)
九年级计算中的关键点
- 取近似值:在九年级的化学计算中,题目通常会明确要求“按表中所给数据计算”或直接使用上表中的简化值(如C=12, O=16),考试时,如果题目给了数据表,以题目给的数据为准;如果没给,则使用上表的简化值。
- 氯(Cl)是特例:氯的相对原子质量精确值约为35.45,但在九年级计算中,必须使用35.5,因为氯气(Cl₂)的分子量是71,使用35.5可以方便地进行计算。
- 计算结果保留:根据有效数字的规则,计算结果的有效位数应与题目中给出的数据保持一致,九年级的计算结果保留到小数点后一位或整数即可。
如何记忆?
死记硬背效果不好,可以尝试以下方法:
- 分类记忆:
- 气体:氢(H,1)、氦(He,4)、氮(N,14)、氧(O,16)、氟(F,19)、氖(Ne,20)、氯(Cl,35.5)、氩(Ar,40)。
- 常见金属:钠(Na,23)、镁(Mg,24)、铝(Al,27)、钾(K,39)、钙(Ca,40)、铁(Fe,56)、铜(Cu,64)、锌(Zn,65)、银(Ag,108)、金(Au,197)、汞(Hg,201)。
- 非金属:碳(C,12)、硅(Si,28)、磷(P,31)、硫(S,32)。
- 数字规律记忆:
- 氢是1,氦是4。
- 第二周期(Li到Ne)的原子质量从7到20,可以按顺序记。
- 第三周期(Na到Ar)的原子质量从23到40,可以按顺序记。
- 铁(Fe)是56,铜(Cu)是64,锌(Zn)是65,银(Ag)是108,金(Au)是197,汞(Hg)是201,这些数字比较有特点,容易记住。
- 联系生活:
- 食盐是氯化钠,记住钠(Na,23)和氯(Cl,35.5)。
- 铁锈是氧化铁,记住铁(Fe,56)和氧(O,16)。
- 加碘盐里有碘,记住碘(I,127)。
相对原子质量有什么用?
它是化学计算的基石,主要用于:
- 计算物质的相对分子质量(或化学式量):
- 公式:相对分子质量 = 化学式中各原子的相对原子质量的总和。
- 示例:计算H₂SO₄的相对分子质量。
- 解:H₂SO₄的相对分子质量 = (1 × 2) + 32 + (16 × 4) = 2 + 32 + 64 = 98
- 计算元素的质量比:
- 示例:计算水中氢元素和氧元素的质量比。
- 解:H₂O中 H : O = (1 × 2) : (16 × 1) = 2 : 16 = 1 : 8
- 示例:计算水中氢元素和氧元素的质量比。
- 计算元素的质量分数:
- 公式:某元素的质量分数 = (该元素的相对原子质量 × 原子个数) / 化合物的相对分子质量 × 100%
- 示例:计算尿素[CO(NH₂)₂]中氮元素的质量分数。
- 解:CO(NH₂)₂的相对分子质量 = 12 + 16 + (14 + 1×2)×2 = 60
- 氮元素的质量分数 = (14 × 2) / 60 × 100% ≈ 7%
希望这份表格和说明对你的学习有帮助!祝你学习进步!









