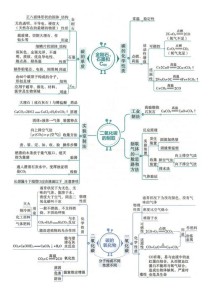
空气究竟由哪些成分组成?
校园之窗 2026年1月27日 23:49:20 99ANYc3cd6
第一部分:空气的组成
空气的成分
空气是一种混合物,它是由多种单一物质组成的,我们可以将其分为两类:
A. 固定成分(按体积分数计算)
这是空气中含量相对稳定、最主要的几种气体。
| 气体名称 | 化学式 | 体积分数 | 主要性质和作用 |
|---|---|---|---|
| 氮气 (N₂) | N₂ | 约 78% | 性质稳定:不燃烧、不支持燃烧(化学性质不活泼)。 作用:作保护气(如灯泡内填充气、食品防腐)、制化肥、硝酸等。 |
| 氧气 (O₂) | O₂ | 约 21% | 性质活泼:支持燃烧、供给呼吸(有助燃性和氧化性)。 作用:动植物呼吸、燃烧、炼钢、气焊等。 |
| 稀有气体 | He, Ne, Ar, Kr, Xe 等 | 约 0.94% | 性质极不活泼(也叫“惰性气体”),一般不与其他物质反应。 作用:作保护气(如焊接金属)、制造电光源(霓虹灯、航标灯等)。 |
| 二氧化碳 (CO₂) | CO₂ | 约 0.03% | 性质:不支持燃烧,也不供给呼吸;参与光合作用。 作用:植物光合作用的原料、灭火、作制冷剂、人工降雨等。 |
B. 可变成分
这些气体的含量会因地区、时间等因素而变化。
- 水蒸气 (H₂O):含量不固定,受天气(湿度)影响很大,从0%到4%不等。
- 其他杂质:如灰尘、二氧化硫 (SO₂)、一氧化碳 (CO)、臭氧 (O₃) 等,这些主要来自工厂废气、汽车尾气、火山喷发等,是空气污染物。
空气中氧气含量的测定实验
这是九年级化学中一个经典且重要的实验,必须熟练掌握。
A. 实验目的
测定空气中氧气的体积分数。
B. 实验原理
利用红磷燃烧消耗密闭容器内的氧气,生成五氧化二磷固体(固体体积几乎不变),导致容器内压强减小,在外界大气压的作用下,水被“压”入容器,进入容器中水的体积约等于消耗的氧气体积。
C. 实验步骤
- 连接装置:将钟罩(或集气瓶、注射器等)与水槽连接,确保装置气密性良好。
- 放入药品:在燃烧匙中放入足量的红磷。
- 点燃反应:用酒精灯点燃红磷后,迅速伸入钟罩内,并立即塞紧橡皮塞。
- 观察现象:
- 红磷剧烈燃烧,产生大量白烟(五氧化二磷固体)。
- 燃烧停止,装置冷却后,钟罩内的水面上升。
- 记录数据:待装置完全冷却后,记录钟罩内水面上升的体积。
- 得出结论:水面上升的体积约占钟罩内空气总体积的 1/5。
D. 实验现象、结论及注意事项
- 实验现象:
- 红磷燃烧,产生大量白烟。
- 装置冷却后,钟罩内水面上升,最终约占容器容积的 1/5。
- 实验结论:
- 空气中氧气的体积约占 1/5。
- 剩余的 4/5 体积主要是氮气,也证明氮气不溶于水,也不与红磷反应。
- 实验成功的关键:
- 气密性要好:否则外界空气会进入,导致水面上升体积偏小。
- 红磷要足量:确保氧气被完全消耗,否则水面上升体积偏小。
- 装置要冷却至室温:否则钟罩内气体温度较高,压强偏大,水会无法完全上升,导致测量结果偏小。
- 不能用木炭或硫代替红磷:因为木炭燃烧生成CO₂(气体),硫燃烧生成SO₂(气体),都会消耗气体,导致容器内外压强差减小,水面几乎不上升,无法测定氧气含量。
- 不能用铁丝代替红磷:因为铁丝在空气中不能燃烧。
第二部分:空气的污染与保护
空气污染物
- 气体污染物:二氧化硫 (SO₂)、一氧化碳、二氧化氮 (NO₂)、臭氧等。
- 可吸入颗粒物:如粉尘、PM2.5(直径小于或等于2.5微米的颗粒物)。
主要来源:
- 化石燃料(煤、石油、天然气)的燃烧。
- 工厂的废气排放。
- 汽车尾气的排放。
- 秸秆焚烧等。
空气污染的危害
- 危害人体健康:引起呼吸道疾病、心血管疾病、肺癌等。
- 形成酸雨:SO₂、NO₂等气体溶于雨水形成,腐蚀建筑物、破坏森林、酸化土壤和水源。
- 破坏臭氧层:氟氯烃等物质会破坏臭氧层,导致紫外线增强,危害皮肤和健康。
- 导致全球气候变暖:二氧化碳等温室气体增多,导致温室效应加剧。
保护空气的措施
- 加强空气质量监测。
- 使用清洁能源:如太阳能、风能、水能、氢能等,代替化石燃料。
- 工厂废气处理达标后排放。
- 改进汽车发动机,安装尾气净化装置。
- 植树造林,绿化环境。
第三部分:混合物与纯净物
根据物质的组成,我们可以将物质分为两大类:
混合物
- 定义:由两种或多种物质混合而成的物质。
- 特点:
- 各物质保持自己原有的化学性质。
- 各物质之间没有发生化学反应。
- 各成分没有固定的比例。
- 不能用化学方法将其中的各物质简单分开。
- 举例:空气、溶液(如盐水、糖水)、合金(如钢、不锈钢)、牛奶等。
纯净物
- 定义:由一种物质组成的物质。
- 特点:
- 具有固定的化学性质。
- 具有固定的组成和性质(如固定的熔点、沸点)。
- 分类:
- 单质:由同一种元素组成的纯净物。
- 举例:氧气 (O₂)、氮气 (N₂)、铁、铜、碳。
- 化合物:由不同种元素组成的纯净物。
- 举例:五氧化二磷 (P₂O₅)、二氧化碳 (CO₂)、水 (H₂O)。
- 单质:由同一种元素组成的纯净物。
总结与要点
- 空气的成分:氮气(78%)、氧气(21%)、稀有气体(0.94%)、二氧化碳(0.03%)、其他气体和杂质(0.03%),记住这些体积分数是常考点。
- 氧气含量的测定实验:是重中之重,要掌握原理、步骤、现象、结论以及实验成败的关键。
- 氮气的性质和作用:不活泼,是主要的保护气。
- 稀有气体:也叫惰性气体,化学性质极不活泼。
- 混合物与纯净物的区别:关键看物质的种类,是“多种”还是“一种”。
- 环境保护:了解空气污染的危害和保护措施,树立环保意识。
希望这份详细的梳理能帮助你全面掌握“空气的组成”这一知识点!祝你学习进步!