九年级化学九单元总结
校园之窗 2026年1月17日 13:00:15 99ANYc3cd6
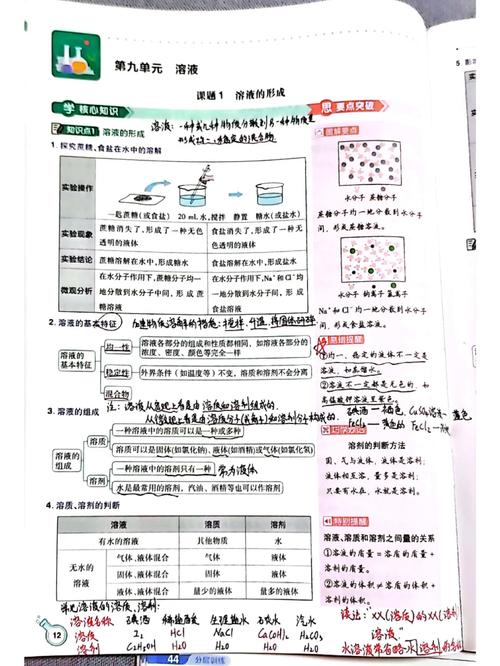
九年级化学第九单元《溶液》全总结
核心概念梳理
溶液的定义、特征和组成
- 定义:一种或几种物质分散到另一种物质中,形成的均一、稳定的混合物。
- 特征:
- 均一性:各部分性质(如密度、浓度、颜色)完全相同。
- 稳定性:在外界条件(温度、溶剂质量)不变时,溶质不会从溶剂中分离出来。
- 混合物:溶液至少由两种物质组成。
- 组成:
- 溶质:被溶解的物质。(可以是固体、液体或气体)
- 溶剂:能溶解其他物质的物质。(水是最常见的溶剂)
- 判断方法:固体、气体溶于液体时,固体/气体是溶质,液体是溶剂,两种液体互溶时,量多的是溶剂,量少的是溶质,若有水存在,水永远是溶剂。
饱和溶液与不饱和溶液

- 定义:
- 饱和溶液:在一定温度下,一定量的溶剂里,不能再溶解某种溶质的溶液。
- 不饱和溶液:在一定温度下,一定量的溶剂里,还能继续溶解某种溶质的溶液。
- 相互转化:
- 不饱和溶液 → 饱和溶液:
- 增加溶质
- 蒸发溶剂(或减少溶剂)
- 改变温度(大多数固体物质的溶解度随温度升高而增大,所以降温;如熟石灰则相反,升温)
- 饱和溶液 → 不饱和溶液:
- 增加溶剂
- 改变温度(大多数固体物质升高温度)
- 不饱和溶液 → 饱和溶液:
- 关键点:讨论饱和与否的前提是“一定温度”和“一定量溶剂”。
溶解度
- 定义:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量(单位:克)。
四要素:①一定温度 ②100克溶剂 ③达到饱和 ④溶解的质量(单位:克)
- 影响溶解度的因素:
- 内因:溶质和溶剂本身的性质。
- 外因:
- 温度:对大多数固体物质,温度越高,溶解度越大(如KNO₃);对少数物质(如熟Ca(OH)₂),温度越高,溶解度越小。
- 压强:对固体、液体溶解度基本无影响;对气体,压强越大,溶解度越大。
- 溶剂种类:同种溶质在不同溶剂中的溶解度不同(如碘在水中难溶,在酒精中易溶)。
- 溶解度曲线:
- 意义:表示物质的溶解度随温度变化的曲线。
- 应用:
- 查找溶解度:查出某物质在某一温度下的溶解度。
- 比较溶解度大小:比较不同物质在同一温度下的溶解度。
- 判断溶解度随温度的变化趋势:曲线越陡,受温度影响越大。
- 确定结晶方法:
- 降温结晶(或冷却热饱和溶液法):适用于溶解度随温度变化较大的物质(如KNO₃)。
- 蒸发溶剂结晶:适用于溶解度随温度变化不大的物质(如NaCl)。
- 确定饱和与不饱和溶液:曲线上的点及下方区域为饱和溶液,曲线上方区域为“过饱和溶液”(不稳定),曲线以上区域为不饱和溶液。
溶质的质量分数
- 定义:溶质质量与溶液质量之比,是表示溶液浓度的一种方法。
- 公式:
- 基本公式:$w = \frac{m{溶质}}{m{溶液}} \times 100\%$
- 推广公式:$w = \frac{m{溶质}}{m{溶质} + m_{溶剂}} \times 100\%$
- 含义:指在100份质量的溶液里,含有多少份质量的溶质,是一个比值,没有单位。
- 饱和溶液的溶质质量分数:
- 在一定温度下,饱和溶液的溶质质量分数是该温度下该物质溶液浓度的最大值。
- 计算公式:$w_{饱和} = \frac{S}{100g + S} \times 100\%$ (其中S为该温度下的溶解度)
重点与难点突破
饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
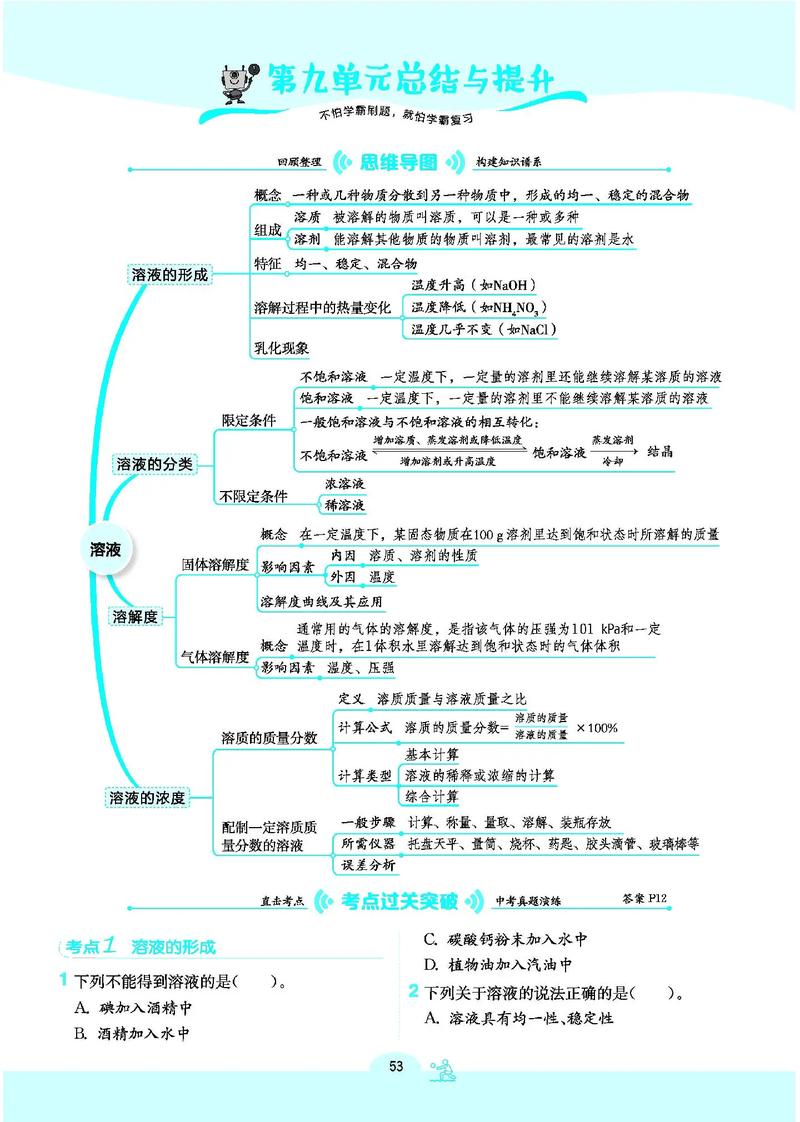
| 概念 | 分类依据 | 关系 |
|---|---|---|
| 饱和/不饱和 | 溶解能力(是否还能继续溶解溶质) | 饱和不一定浓,不饱和不一定稀。 在一定温度下,熟石灰的饱和溶液很稀;而蔗水的不饱和溶液可以很浓。 |
| 浓/稀溶液 | 浓度大小(溶质质量分数的大小) | 只有在同种溶质、同种温度下,才能说“饱和溶液一定比不饱和溶液浓”。 |
溶解度曲线上的“点、线、面”
- 点:
- 交点:表示在该温度下,两种物质的溶解度相等。
- 曲线上的点:表示该温度下对应的饱和溶液。
- 曲线下方的点:表示该温度下的不饱和溶液。
- 线:
- 曲线的陡峭程度:曲线越陡,溶解度受温度影响越大。
- 曲线的走势:大多数物质“陡升”,少数物质(如熟石灰)“下降”。
- 面:
- 曲线上方(含曲线):饱和溶液。
- 曲线下方:不饱和溶液。
关于溶液的计算(核心难点)
- 基本类型:
- 已知溶质和溶剂质量,求溶质质量分数。 $w = \frac{m{溶质}}{m{溶质} + m_{溶剂}} \times 100\%$
- 配制一定溶质质量分数的溶液(实验操作)。
- 仪器:托盘天平(带砝码)、药匙、烧杯、玻璃棒、量筒、胶头滴管。
- 步骤:计算 → 称量(或量取)→ 溶解 → 装瓶贴签。
- 玻璃棒的作用:搅拌,加速溶解。
- 溶液稀释或浓缩的计算。
- 核心公式:稀释前后,溶质的质量不变。
- $m{浓} \times w{浓} = m{稀} \times w{稀}$
- 或 $m{浓} \times w{浓} = (m{浓} + m{加水}) \times w_{稀}$
- 涉及化学反应的溶液计算。
- 解题关键:根据化学方程式求出生成物(溶质)的质量,再结合溶液质量进行计算。
- 溶液质量:通常指所有反应物的总质量 - 生成的沉淀质量 - 生成的气体质量。
- 注意:若反应物中有不溶物,则不溶物质量不计入溶液质量。
常见误区与易错点
- 混淆溶液、溶质、溶剂:将“碘酒”中的碘误认为是溶剂,酒精是溶质。(正确:碘是溶质,酒精是溶剂)。
- 忽略饱和溶液的前提条件:忘记“一定温度”和“一定量溶剂”这两个前提。
- 对溶解度概念理解不清:将100克溶液误认为是100克溶剂;忘记单位是“克”而不是“%”。
- 混淆浓溶液与饱和溶液:认为浓溶液就是饱和溶液,稀溶液就是不饱和溶液。
- 计算溶液质量时出错:
- 将水的体积直接当作水的质量(需用密度换算,但题目常忽略密度,视为1g/mL)。
- 在化学反应中,忘记减去生成的沉淀或气体的质量。
- 配制溶液的操作错误:
- 用天平称量固体时,药品和砝码放反了。
- 用量筒配制溶液时,俯视或仰视读数导致体积不准。
- 溶解时未用玻璃棒搅拌,或搅拌时碰到烧杯壁。
典型例题解析
概念辨析
例:下列说法正确的是( ) A. 饱和溶液一定是浓溶液 B. 均一、稳定的液体一定是溶液 C. 氨气的水溶液中,氨气是溶质,水是溶剂 D. 降低饱和溶液的温度,一定有晶体析出
解析: A. 错误,如熟石灰的饱和溶液很稀。 B. 错误,如水是均一、稳定的液体,但它是纯净物,不是溶液。 C. 正确,气体溶于液体,气体是溶质。 D. 错误,对于溶解度随温度降低而减小的物质(如KNO₃),会析出晶体;但对于溶解度随温度降低而增大的物质(如熟石灰),则不会析出晶体,反而会变成不饱和溶液。
答案:C
溶解度曲线应用
例:如图是A、B、C三种固体物质的溶解度曲线,请回答: (1) t₂℃时,A、B、C三种物质的溶解度由大到小的顺序是 __________。 (2) t₁℃时,将30g A物质加入到50g水中,充分溶解后,所得溶液的质量为 __________ g。 (3) 将t₂℃时A、B、C三种物质的饱和溶液降温至t₁℃,所得溶液中溶质质量分数由大到小的顺序是 __________。
解析: (1) 比较同一温度下不同物质的溶解度,直接看曲线的高低,t₂℃时,B的曲线最高,C次之,A最低,所以顺序是 B > C > A。 (2) t₁℃时,A的溶解度是20g,即在100g水中最多溶解20g A,现在50g水最多溶解10g A,加入的30g A有20g未溶解,所以溶液质量 = 溶质质量 + 溶剂质量 = 10g + 50g = 60g。 (3) 降温后,分析各溶液的变化:
- A:溶解度减小,会析出晶体,溶质质量分数变小,但t₁℃时A的饱和溶液溶质质量分数是 $\frac{20}{100+20} \times 100\% \approx 16.7\%$。
- B:溶解度减小,会析出晶体,t₁℃时B的溶解度是40g,溶质质量分数是 $\frac{40}{100+40} \times 100\% \approx 28.6\%$。
- C:溶解度增大,变为不饱和溶液,溶质、溶剂质量不变,溶质质量分数是 $\frac{30}{100+30} \times 100\% \approx 23.1\%$。
- 比较降温后的溶质质量分数:B > C > A。
答案:(1) B > C > A (2) 60 (3) B > C > A
溶液计算
例:将100g 9.8%的稀硫酸与足量锌粒完全反应,求: (1) 生成氢气的质量。 (2) 反应后所得溶液中溶质的质量分数。
解析: (1) 设生成氢气的质量为x,生成硫酸锌的质量为y。 $Zn + H_2SO_4 = ZnSO_4 + H_2 \uparrow$ 98 161 2 100g × 9.8% = 9.8g y x
$\frac{98}{9.8g} = \frac{2}{x}$ 解得 $x = 0.2g$ $\frac{98}{9.8g} = \frac{161}{y}$ 解得 $y = 16.1g$
(2) 反应后溶液的质量 = 反应前所有物质的总质量 - 生成的气体质量 = 100g (稀硫酸) + 足量锌粒 - 0.2g (氢气) 因为锌粒是“足量”,但反应中消耗的锌的质量为 $\frac{65}{98} \times 9.8g = 6.5g$,所以更精确的计算是: = 100g + 6.5g - 0.2g = 106.3g
溶质质量分数 = $\frac{溶质质量}{溶液质量} \times 100\% = \frac{16.1g}{106.3g} \times 100\% \approx 15.2\%$
答案:(1) 生成氢气0.2g。(2) 反应后所得溶液中溶质的质量分数约为15.2%。
学习建议
- 构建知识网络:将溶液的定义、组成、饱和与不饱和、溶解度、溶质质量分数等概念串联起来,形成知识体系。
- 重视实验:亲手操作“配制一定溶质质量分数的溶液”实验,理解每一步操作的目的和注意事项。
- 勤于归纳:总结溶解度曲线的“点线面”规律、结晶方法的选择、溶液计算的常用公式和技巧。
- 多做题,多反思:通过练习巩固概念,特别是对于易错点,要反复琢磨,找出错误原因,避免再犯。
希望这份总结对你有帮助!祝你学习进步!