化学式与化合价,如何快速掌握?
校园之窗 2026年1月14日 03:27:02 99ANYc3cd6
第一部分:化合价
你可以把化合价理解为元素在形成化合物时表现出的一种“身价”或“化合能力”,它决定了不同原子之间以什么样的比例结合。
为什么要学化合价?
因为原子结合成分子时,它们的数量不是随意的,而是遵循一定的规律,这个规律就是由化合价来规定的。化合物中正负化合价的代数和为零,这是化合价最核心、最重要的应用。

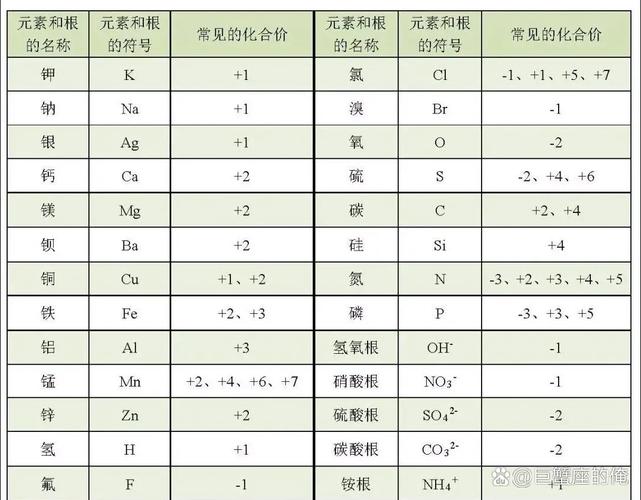
常见元素的化合价(必须背诵!)
这是最枯燥也最关键的一步,没有捷径,只能反复记忆,下面是帮你记忆的口诀和表格:
常见元素化合价口诀:
一价氢氯钾钠银, 二价氧钙钡镁锌, 三铝四硅五价磷, 二三铁,二四碳, 二四六硫都齐全, 铜汞二价最常见。
详细表格(请务必熟记):

| 元素名称 | 元素符号 | 常见化合价 | 备注 |
|---|---|---|---|
| 氢 | H | +1 | 通常为+1,在金属氢化物中为-1(如NaH) |
| 氧 | O | -2 | 通常为-2,在过氧化物中为-1(如H₂O₂) |
| 钾、钠 | K, Na | +1 | |
| 银 | Ag | +1 | |
| 钙、镁、钡 | Ca, Mg, Ba | +2 | |
| 锌 | Zn | +2 | |
| 铝 | Al | +3 | |
| 氯 | Cl | -1, +1, +5, +7 | -1最常见,如NaCl |
| 溴、碘 | Br, I | -1 | |
| 硫 | S | -2, +4, +6 | -2在硫化物中(如H₂S),+4在SO₂中,+6在H₂SO₄中 |
| 碳 | C | +2, +4 | +4最常见,如CO₂ |
| 氮 | N | -3, +3, +5 | -3在NH₃中,+5在HNO₃中 |
| 铁 | Fe | +2, +3 | 亚铁显+2(Fe²⁺),铁显+3(Fe³⁺) |
| 铜 | Cu | +1, +2 | +2更常见 |
化合价的规则(非常重要!)
- 化合物中正负化合价代数和为零。(这是黄金法则!)
- 单质中,元素的化合价为零。(因为没有得失电子,如O₂、Fe、H₂)
- 在化合物中,通常氧显-2价,氢显+1价。
- 在化合物中,金属元素通常显正价,非金属元素通常显负价。(但非金属元素与氧或活泼金属结合时显正价,如CO₂中的C显+4价)
第二部分:化学式
化学式是用元素符号和数字的组合来表示物质组成的式子,它就像一个“分子身份证”,告诉我们:
- 这种物质由哪些元素组成。
- 这些元素原子的个数比是多少。
化学式的意义(以 H₂O 为例)
| 意义 | 化学式 H₂O 表示 |
|---|---|
| 宏观 | ① 表示水这种物质。 ② 表示水是由氢元素和氧元素组成的。 |
| 微观 | ① 表示一个水分子。 ② 表示一个水分子是由2个氢原子和1个氧原子构成的。 |
化学式的书写规则
化学式的书写是化合价最直接的应用,核心原则就是:正价前,负价后,化合价交叉化简,写在元素符号右下角。
步骤:
- 排序:按正价元素在前,负价元素在后的顺序写出元素符号。
- 标价:在元素符号正上方标出其常见化合价。
- 交叉:将化合价的绝对值交叉作为对方原子个数。
- 化简:若交叉后得到的数字能约分(如2和2约成1和1),则必须约分。
- 检查:根据化合物中正负化合价代数和为零进行验证。
举例:
-
氧化铝
- 排序:Al O
- 标价: $\overset{+3}{Al}$ $\overset{-2}{O}$
- 交叉: $\overset{+3}{Al}$ $\overset{-2}{O}$ → Al₂O₃
- 化简:数字2和3互质,无需化简。
- 检查: (+3) × 2 + (-2) × 3 = 6 - 6 = 0,正确!
-
碳酸钠 (这是一个特例,需要知道原子团)
- 原子团:由多个原子构成的原子集团,在化合物中作为一个整体,带有固定的化合价。
- 碳酸根 (CO₃²⁻):-2价
- 硫酸根 (SO₄²⁻):-2价
- 氢氧根 (OH⁻):-1价
- 铵根 (NH₄⁺):+1价
- 排序:Na CO₃
- 标价: $\overset{+1}{Na}$ $\overset{-2}{CO_3}$
- 交叉: $\overset{+1}{Na}$ $\overset{-2}{CO_3}$ → Na₂CO₃
- 化简:数字2和1互质,无需化简。
- 检查: (+1) × 2 + (-2) × 1 = 2 - 2 = 0,正确!
- 原子团:由多个原子构成的原子集团,在化合物中作为一个整体,带有固定的化合价。
化学式的读法
读法与写法相反,一般从右向左读。
- 氧化物:“氧化某”或“几氧化几某”
- MgO → 氧化镁
- CO₂ → 二氧化碳
- Fe₂O₃ → 三氧化二铁
- 由金属和非金属组成:“某化某”
- NaCl → 氯化钠
- FeCl₃ → 氯化铁
- 含原子团的化合物:“某酸某”或“几某酸某”
- CaCO₃ → 碳酸钙
- Na₂SO₄ → 硫酸钠
- Fe(OH)₃ → 氢氧化铁
第三部分:化合价与化学式的综合应用
这是考试的重点和难点,主要分为两大类:
根据化学式计算某元素的化合价
核心思路:利用 化合物中正负化合价代数和为零 这个原则,列方程求解。
例题:计算 KClO₃ 中氯元素的化合价。
- 设未知数:设Cl元素的化合价为x。
- 列出已知信息:
- K的化合价为+1
- O的化合价为-2
- Cl的化合价为x
- 根据法则列方程: (+1) + x + (-2) × 3 = 0
- 解方程: 1 + x - 6 = 0 x = 5
- 得出结论:KClO₃中氯元素的化合价为+5价。
根据化合价书写化学式
这就是我们前面讲的“化学式的书写规则”,是必考题型。
例题:写出硫酸亚铁的化学式。
- 找出元素和原子团:
- 阳离子:亚铁离子 (Fe²⁺),化合价为+2
- 阴离子:硫酸根离子 (SO₄²⁻),化合价为-2
- 排序:正价在前,负价在后 → Fe SO₄
- 标价: $\overset{+2}{Fe}$ $\overset{-2}{SO_4}$
- 交叉: $\overset{+2}{Fe}$ $\overset{-2}{SO_4}$ → FeSO₄
- 化简:数字2和2约分为1和1,省略不写。
- 检查: (+2) × 1 + (-2) × 1 = 0,正确!
学习建议与技巧
- 先背后用,熟能生巧:先花时间把常见元素的化合价口诀背得滚瓜烂熟,这是所有应用的基础。
- 理解“代数和为零”:不要死记硬背,要深刻理解这个核心法则,无论是计算化合价还是写化学式,都是在围绕这个法则做文章。
- 多做练习,举一反三:找一些典型的题目来练习,特别是根据化合价写化学式和根据化学式求化合价这两种题型,做到一看题目就知道解题思路。
- 制作卡片:把易混淆的元素(如Fe²⁺和Fe³⁺)、特殊的物质(如H₂O₂、NH₃)做成小卡片,随时拿出来看。
- 建立联系:把化学式和后面的化学方程式联系起来,你会发现化学式是方程式的基础,学好它,方程式也就不难了。
化合价是规则,化学式是规则的应用。 只要你掌握了常见元素的化合价,并能熟练运用“代数和为零”的原则,这部分内容就基本攻克了,祝你学习进步,化学成绩节节高!




