九年级化学实验探究题怎么解?
校园之窗 2026年1月31日 05:55:16 99ANYc3cd6
下面我将为你系统地梳理这类题型的核心考点、解题策略、经典题型示例和答题模板,助你攻克这一难关。
核心考点与能力要求
实验探究题通常围绕一个核心问题展开,需要你运用所学知识,经历完整的科学探究过程,主要考点包括:
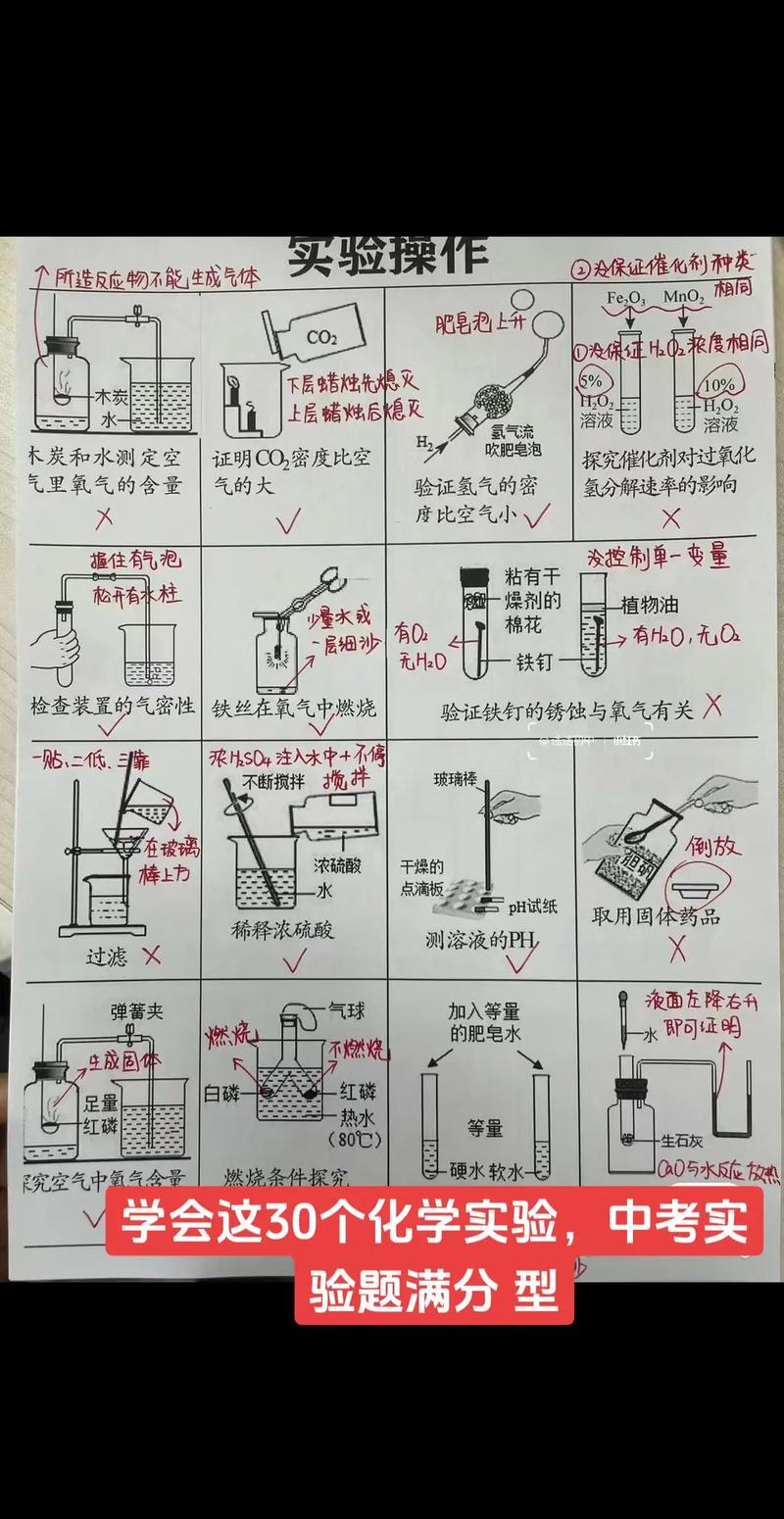
- 实验基本操作:仪器识别、药品取用、加热、过滤、蒸发、气密性检查等。
- 气体的制取与净化:
- 发生装置:固固加热型(如制O₂)、固液不加热型(如制CO₂、H₂)。
- 收集装置:排水法(难/不易溶于水)、向上排空气法(密度比空气大)、向下排空气法(密度比空气小)。
- 净化:除杂(长进短出)、干燥(通常用浓硫酸或碱石灰)。
- 物质的性质与检验:
- 常见气体的检验(O₂、CO₂、H₂、CO等)。
- 常见离子的检验(Cl⁻、SO₄²⁻、CO₃²⁻、NH₄⁺等)。
- 酸、碱、盐的化学性质。
- 实验设计与评价:
- 变量控制:探究某个因素对实验结果的影响时,要控制其他变量相同。
- 对比实验:通过设置对照组,得出科学结论。
- 实验方案的合理性、安全性、环保性评价。
- 实验结论与反思:
- 根据实验现象,正确书写化学方程式。
- 分析实验失败的原因。
- 对实验方案进行改进或提出新的探究问题。
解题“四步走”战略
遇到实验探究题,不要急于下笔,按照以下四个步骤,思路会清晰很多:
第一步:审题干,抓核心
- 做什么? 快速浏览题目,找出实验探究的核心问题是什么,是验证某个猜想?是探究某个反应的原理?还是比较不同物质的性质?
- 给什么? 圈出题目中给出的所有信息:实验目的、药品、仪器、已知的实验步骤、现象等,这些都是解题的“已知条件”。
- 考什么? 思考这道题主要考察哪个或哪几个知识点(如气体制备、酸的性质、金属活动性顺序等)。
第二步:联知识,想原理
- 将核心问题与你脑中的化学知识库建立联系。
- 探究“铁生锈的条件”,就要立刻联想到铁生锈是铁与氧气、水共同作用的结果。
- 要“除去CO₂中的少量CO”,就要想到CO具有可燃性或还原性,而CO₂没有,可以利用这个性质差异来除杂。
第三步:析过程,答问题
这是解题的关键环节,要分模块、有条理地回答问题。
- 装置问题:根据反应物状态和反应条件选择发生装置;根据气体密度和溶解性选择收集装置。
- 现象描述:“先...后...”、“有...生成”、“由...色变为...色”,描述要准确、完整,不要遗漏。
- 结论得出:“根据...现象,说明...”,结论必须与现象直接对应,并且要用化学术语表达。
- 化学方程式:书写要规范,注意配平、条件、沉淀/气体符号。
- 方案设计/评价:
- 设计:明确实验目的,控制变量,设置对照组,描述现象,得出结论。
- 评价:从科学性(原理是否正确)、可行性(操作是否简单)、安全性(是否危险)、环保性(是否污染环境)等角度分析。
第四步:查细节,防失误
- 检查化学式、化学方程式是否正确。
- 检查语言描述是否清晰、准确,有无错别字。
- 检查单位、符号是否规范。
- 检查是否所有问题都已回答。
经典题型与示例分析
探究物质成分
通常给出混合物或未知物,要求通过实验推断其成分。
【示例】 有一包白色粉末,可能是碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种,某同学为了探究其成分,做了如下实验:

| 实验步骤 | 实验现象 | |
|---|---|---|
| 取少量粉末于试管中,加入足量水,振荡 | 粉末全部溶解,得到无色溶液 | 一定不含__(填化学式) |
| 向上述溶液中滴加足量稀硝酸 | 有气泡产生 | 一定含有__(填化学式) |
| 向步骤2后的溶液中滴加硝酸钡溶液 | 有白色沉淀生成 | 一定含有__(填化学式) |
【解题思路】
- 审题干:探究白色粉末的成分,可能含Na₂CO₃、Na₂SO₄、NaCl、NaOH。
- 联知识:
- 题目涉及离子的检验:CO₃²⁻(用酸检验,产生CO₂)、SO₄²⁻(用Ba²⁺检验,生成BaSO₄沉淀)、Cl⁻(用Ag⁺检验,生成AgCl沉淀)。
- 溶液颜色:Cu²⁺(蓝)、Fe³⁺(黄),本题无色,排除了有颜色的离子。
- 析过程:
- 步骤1:粉末全部溶解,得到无色溶液。
- 碳酸钠、硫酸钠、氯化钠、氢氧化钠都溶于水。
- 但如果含有碳酸钠和氢氧化钠的混合物,加水后也会溶解,这个现象只能说明粉末中不含不溶于水的物质(本题中没给),但无法直接排除任何一种,通常这个步骤是为了排除不溶性杂质,我们继续看下一步。
- 修正思路:步骤1的现象主要是为了说明溶液中不含会形成有色沉淀的离子,但本题中所有物质溶解后都无色,所以这个步骤的关键信息是“全部溶解”,说明没有不溶物,我们结合后续步骤判断。
- 步骤2:滴加足量稀硝酸,有气泡产生。
- 产生气泡,说明溶液中含CO₃²⁻,因为CO₃²⁻ + 2H⁺ = CO₂↑ + H₂O。
- 粉末中一定含有碳酸钠(Na₂CO₃)。
- 加入足量稀硝酸后,碳酸钠完全反应生成CO₂和水,溶液中的CO₃²⁻被除去。
- 步骤3:向步骤2后的溶液中滴加硝酸钡溶液,有白色沉淀生成。
- 步骤2后,溶液中只剩下NaNO₃和可能存在的其他物质的反应产物。
- 能与Ba²⁺生成白色沉淀的离子是SO₄²⁻,因为Ba²⁺ + SO₄²⁻ = BaSO₄↓。
- 这个SO₄²⁻只能来自原始粉末中的硫酸钠(Na₂SO₄)。
- 注意:如果原始粉末中只有碳酸钠,步骤2加酸后不会有沉淀生成,现在有沉淀,说明一定有硫酸钠。
- 步骤1:粉末全部溶解,得到无色溶液。
- 查细节:
氯化钠和氢氧化钠的存在与否无法确定,因为氯化钠不与稀硝酸、硝酸钡反应;氢氧化钠会与稀硝酸反应生成硝酸钠,但硝酸钠也不与硝酸钡反应,结论只能说“一定含有”和“一定不含有”的物质。
【参考答案】
- 一定不含:无(或无法确定,但通常第一步是排除不溶物,本题中所有物质都溶,所以填“无”或“无法确定”)。(更正:结合后续步骤,第一步主要说明溶液澄清,无杂质,关键信息在后续)
- 一定含有:Na₂CO₃
- 一定含有:Na₂SO₄
(更严谨的分析)
- 步骤1:粉末全部溶解,得到无色溶液,说明没有不溶性杂质,且溶液中无Cu²⁺、Fe³⁺等有色离子。(本题中所有可能物质都符合)
- 步骤2:滴加足量稀硝酸,有气泡产生。证明原粉末中一定含有Na₂CO₃。
- 步骤3:向步骤2后的溶液中滴加硝酸钡溶液,有白色沉淀生成,此沉淀是BaSO₄。证明原粉末中一定含有Na₂SO₄。
- 关于NaOH和NaCl:无法确定是否存在,因为NaOH会与HNO₃反应,NaCl不参与反应,它们的存在与否不影响现象。
探究反应规律或影响因素
通常以“影响XX反应速率的因素是什么?”或“金属与酸反应的规律是什么?”等形式出现。
【示例】 某化学兴趣小组探究“影响过氧化氢(H₂O₂)分解速率的因素”。 【提出猜想】 猜想一:与催化剂有关。 猜想二:与过氧化氢溶液的浓度有关。 【设计并进行实验】 | 实验编号 | 过氧化氢溶液浓度 | 催化剂 | 收集50mL氧气所需时间 | | :--- | :--- | :--- | :--- | | ① | 5% | 无 | 很长时间 | | ② | 5% | 二氧化锰 | 5秒 | | ③ | 10% | 二氧化锰 | 3秒 |
(1) 通过实验①和②,可验证猜想__,结论是__。 (2) 要验证猜想二,应选择的实验是__(填编号)。 (3) 某同学提出,还可能与“反应温度”有关,请设计一个简单的实验方案来验证你的猜想:__。
【解题思路】
- 审题干:核心问题是探究影响H₂O₂分解速率的因素,猜想有催化剂和浓度。
- 联知识:H₂O₂在MnO₂催化下分解生成水和氧气,2H₂O₂ $\xrightarrow{MnO₂}$ 2H₂O + O₂↑,反应速率快慢可以通过产生气体的快慢来衡量。
- 析过程:
- (1) 实验①和②,除了“催化剂”这个条件不同(①无,②有MnO₂),其他条件(浓度5%)都相同,实验②收集氧气的时间远小于实验①,说明MnO₂能加快反应速率,所以验证的是猜想一,结论是:催化剂可以加快过氧化氢的分解速率。
- (2) 要验证猜想二(浓度的影响),需要保证“催化剂”相同,改变“浓度”,实验②和③,催化剂都是MnO₂,浓度分别是5%和10%,所以选择②和③。
- (3) 设计实验探究“温度”的影响,根据控制变量法,需要保证“浓度”和“催化剂”相同,改变“温度”。
- 方案:取两份相同浓度(如5%)的过氧化氢溶液,其中一份放在冰水浴中(低温),另一份放在热水浴中(高温),同时加入相同质量的二氧化锰,比较收集相同体积氧气所需的时间,若高温所需时间短,则说明温度越高,反应速率越快。
- 查细节:描述实验方案时,要清晰说明控制哪些变量,改变哪个变量,观察什么现象。
【参考答案】 (1) 一; 催化剂可以加快过氧化氢的分解速率。 (2) ②和③ (3) 取两份等浓度(如5%)的过氧化氢溶液,分别放入冰水浴(或冷水)和热水中,再加入相同质量的二氧化锰,观察并比较产生气泡的速率(或收集等量氧气所需的时间)。
答题技巧与注意事项
- 术语要规范:不要用口语化表达,说“冒泡”不如说“产生气泡”;说“烧杯变热”不如说“放出热量”。
- 现象要全面:描述现象时,要包括“反应物、生成物、能量变化、颜色、气味、状态”等,镁条在空气中燃烧:发出耀眼白光,放出大量热,生成一种白色固体。
- 结论要对应:结论必须从现象中得出,不能凭空想象,看到澄清石灰水变浑浊,结论是“生成了二氧化碳”,而不是“证明是碳”。
- 变量要控制:在设计实验时,这是最容易出错的地方,一定要想清楚,除了要探究的那个因素,其他所有条件都必须保持一致。
- 安全记心中:在评价或设计实验时,要考虑到安全性,点燃可燃性气体前要验纯;实验室禁止品尝药品等。
希望这份详细的指南能帮助你系统地掌握九年级化学实验探究题的解题方法,多加练习,总结反思,你一定能攻克这个难关!祝你学习进步!



