溶液浓度怎么算?溶质溶剂啥关系?
校园之窗 2026年1月30日 04:42:37 99ANYc3cd6
核心概念:什么是溶液的浓度?
溶液的浓度:是指一定量的溶液里所含溶质的量,就是溶液的“浓”或“稀”的程度。
它是一个相对量,不是一个绝对量,10克糖溶解在90克水里,和20克糖溶解在180克水里,浓度是相同的,都是10%。

表示溶液浓度的常见方法(九年级重点)
九年级化学主要掌握以下两种表示方法:
溶质的质量分数
这是九年级化学中最重要、最核心的浓度表示方法。
(1)定义与公式
-
定义:溶质的质量分数是溶质的质量与溶液的质量之比。
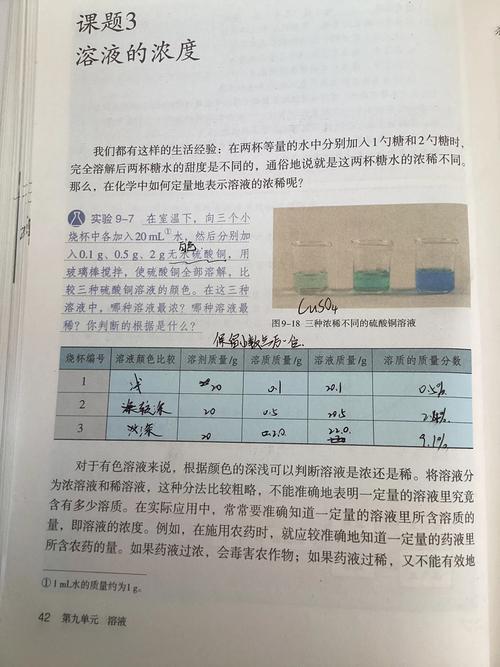 (图片来源网络,侵删)
(图片来源网络,侵删) -
公式:
溶质的质量分数 = (溶质的质量 / 溶液的质量) × 100%
- 溶液的质量 = 溶质的质量 + 溶剂的质量
(2)关键点解析
- “质量”是关键:溶质质量、溶剂质量、溶液质量都必须用质量(单位通常是克g)来表示。
- 溶质的质量:指已溶解的溶质的质量,如果题目说“将10g NaCl放入水中,有2g未溶解”,那么溶质的质量就是 10g - 2g = 8g。
- 溶液的质量:溶液的质量可以通过称量得到,也可以通过“溶质质量 + 溶剂质量”计算得到。特别注意:溶液的质量不等于溶剂的体积加上溶质的体积,因为分子间有间隔。
- 无单位:质量分数是一个比值,没有单位,通常用百分数(%)表示。
(3)常用计算类型

已知溶质和溶剂的质量,求溶质的质量分数。
例题:将25g氯化钠完全溶解在125g水中,求所得溶液的溶质质量分数。 解析:
- 溶质质量 = 25g
- 溶剂质量 = 125g
- 溶液质量 = 25g + 125g = 150g
- 溶质质量分数 = (25g / 150g) × 100% ≈ 16.7%
配制一定溶质质量分数的溶液(实验操作) 这是中考实验题的常考点,步骤和仪器要记牢。
-
步骤:
- 计算:计算所需溶质和溶剂的质量。
- 溶质质量 = 所需溶液质量 × 溶质质量分数
- 溶剂质量 = 所需溶液质量 - 溶质质量
- 称量:用托盘天平称量所需质量的固体溶质。
- 量取:用量筒量取所需体积的液体溶剂。(注意:水的密度按1g/cm³计算,即1mL水≈1g水)
- 溶解:将称好的溶质倒入烧杯中,再倒入量取的溶剂,用玻璃棒搅拌,使溶质完全溶解。
- 计算:计算所需溶质和溶剂的质量。
-
仪器:托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管。
-
玻璃棒的作用:搅拌,加速溶解,防止局部过热。
溶液的稀释或浓缩
- 核心原理:在稀释或浓缩过程中,溶质的质量保持不变。
稀释前溶质质量 = 稀释后溶质质量 m(浓溶液) × w(浓) = m(稀溶液) × w(稀)
例题:用50g 20%的氯化钠溶液配制10%的氯化钠溶液,需要加水多少克? 解析:
- 设需要加水的质量为x。
- 稀释前溶质质量 = 50g × 20% = 10g
- 稀释后溶液总质量 = 50g + x
- 稀释后溶质质量 = (50g + x) × 10%
- 根据原理:10g = (50g + x) × 10%
- 解得:x = 50g
- 答:需要加水50克。
溶液中某元素的质量分数
这是一种特殊的溶质质量分数,计算时溶质是化合物中特定元素的质量。
公式:
某元素的质量分数 = (该元素的相对原子质量 × 原子个数 / 化合物的相对分子质量) × 100%
例题:计算硝酸铵(NH₄NO₃)中氮元素的质量分数。 解析:
- NH₄NO₃的相对分子质量 = 14 + 1×4 + 14 + 16×3 = 80
- 氮元素的总质量 = 14 × 2 = 28
- 氮元素的质量分数 = (28 / 80) × 100% = 35%
- 这意味着,每100g硝酸铵中,含有35g的氮元素。
重要概念辨析
-
饱和溶液 vs. 不饱和溶液
- 饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能再继续溶解时,所得到的溶液。
- 不饱和溶液:还能继续溶解更多溶质的溶液。
- 关键点:
- “饱和”与“不饱和”的前提是指明温度和溶剂的量。
- 饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液,熟石灰在常温下溶解度很小,其饱和溶液很稀;而蔗糖在常温下溶解度很大,其不饱和溶液可以很浓。
-
浓溶液 vs. 稀溶液
- 这是一个定性描述,指溶质质量分数相对较大或较小的溶液。
- 它与溶液是否饱和没有必然联系。
-
溶解度
- 定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,单位是“克”。
- 与溶质质量分数的关系:
一定温度下,某饱和溶液的溶质质量分数 = (溶解度 / (100g + 溶解度)) × 100%
- 例题:20℃时,氯化钠的溶解度是36g,求该温度下饱和氯化钠溶液的溶质质量分数。
解析:
- 溶质质量 = 36g
- 溶剂质量 = 100g
- 溶液质量 = 100g + 36g = 136g
- 溶质质量分数 = (36g / 136g) × 100% ≈ 26.5%
中考常见考点与技巧
- 图像题:分析溶解度曲线,判断溶解度随温度的变化,比较不同物质溶解度的大小,判断结晶的方法(蒸发溶剂或降温结晶)。
- 实验探究题:考查溶液配制的步骤、误差分析。
- 称量时左码右物 → 溶质偏小 → 质量分数偏小。
- 俯视量筒读数 → 溶剂偏少 → 质量分数偏大。
- 未将烧杯中的溶液全部转移到容量瓶 → 溶质偏少 → 质量分数偏小。
- 综合计算题:常将化学方程式的计算与溶质质量分数的计算结合。关键步骤:
- 根据化学方程式求出生成物(溶质)的质量。
- 根据题目信息求出反应后溶液的总质量(常用方法:反应物总质量 - 生成沉淀/气体的质量)。
- 最后用公式 溶质质量分数 = (溶质质量 / 溶液质量) × 100% 求解。
| 概念/方法 | 定义/公式 | 关键点 |
|---|---|---|
| 溶质的质量分数 | (溶质质量 / 溶液质量) × 100% | ① 质量,不是体积 ② 溶质是“已溶解”的量 ③ 溶液质量 = 溶质+溶剂 |
| 溶液配制 | 计算 → 称量 → 量取 → 溶解 | ① 仪器:天平、量筒、烧杯、玻璃棒 ② 玻璃棒作用:搅拌 |
| 溶液稀释 | m(浓) × w(浓) = m(稀) × w(稀) | 核心:稀释过程中溶质质量不变 |
| 元素质量分数 | (元素总质量 / 化合物质量) × 100% | 计算化合物中特定元素的含量 |
| 饱和溶液溶质质量分数 | (溶解度 / (100g + 溶解度)) × 100% | 必须是饱和溶液,且温度固定 |
希望这份详细的梳理能帮助你彻底理解溶液的浓度!学习时多动手计算,多总结错题,一定能攻克这个难点。