九年级化学物质分类如何区分纯净物与混合物?
校园之窗 2026年1月11日 07:13:24 99ANYc3cd6
九年级化学物质分类总览
我们可以从一个简单的树状图来理解整个分类体系:
物质
├── 纯净物
│ ├── 单质
│ │ ├── 金属单质 (如: Fe, Cu, Al)
│ │ ├── 非金属单质 (如: O₂, S, C)
│ │ └── 稀有气体单质 (如: He, Ne)
│ └── 化合物
│ ├── 无机化合物
│ │ ├── 氧化物 (如: H₂O, CuO)
│ │ ├── 酸 (如: H₂SO₄, HCl)
│ │ ├── 碱 (如: NaOH, Ca(OH)₂)
│ │ └── 盐 (如: NaCl, CaCO₃)
│ └── 有机化合物 (初中阶段只要求了解最简单的: CH₄, C₂H₅OH)
└── 混合物
├── 均一混合物 (溶液) (如: 食盐水, 糖水)
└── 非均一混合物 (悬浊液、乳浊液) (如: 泥水, 牛奶)纯净物 vs. 混合物
这是物质分类的最高层次,判断依据是物质的种类。
(图片来源网络,侵删)
| 分类 | 定义 | 特点 | 举例 |
|---|---|---|---|
| 纯净物 | 由一种物质组成。 | - 有固定的组成和性质(如固定的熔点、沸点)。 - 可用化学式表示。 |
氧气(O₂)、水(H₂O)、二氧化碳(CO₂)、氯化钠(NaCl) |
| 混合物 | 由两种或多种物质混合而成。 | - 没有固定的组成和性质。 - 各成分保持各自的化学性质。 - 可用物理方法分离。 |
空气、溶液(如食盐水)、合金(如钢)、牛奶 |
【关键区分】
- 宏观:看是否由一种物质组成。
- 微观:看是否由同一种分子构成(对由分子构成的物质而言)。
纯净物的分类
纯净物根据其元素的组成,分为单质和化合物。
单质
定义:由同一种元素组成的纯净物。
| 分类 | 定义 | 常见例子 | 化学性质 |
|---|---|---|---|
| 金属单质 | 由金属元素组成的单质。 | 铁、铜、铝、锌、金、银 | 一般具有金属光泽、导电性、导热性、延展性;能与氧气、酸等反应。 |
| 非金属单质 | 由非金属元素组成的单质。 | 氧气(O₂)、氮气(N₂)、氢气(H₂)、碳、硫、磷 | 性质多样,如氧气助燃,氮气化学性质稳定,碳有可燃性和还原性。 |
| 稀有气体单质 | 由稀有气体元素组成的单质。 | 氦、氖、氩等 | 化学性质非常稳定,通常不与其他物质反应。 |
【注意】

(图片来源网络,侵删)
- 元素是宏观概念,只讲种类,不讲个数。 水中含有氢元素和氧元素。
- 原子是微观概念,既讲种类,也讲个数。 一个水分子由两个氢原子和一个氧原子构成。
化合物
定义:由不同种元素组成的纯净物。
九年级重点学习的是无机化合物,并根据其性质特点分为氧化物、酸、碱、盐四类。
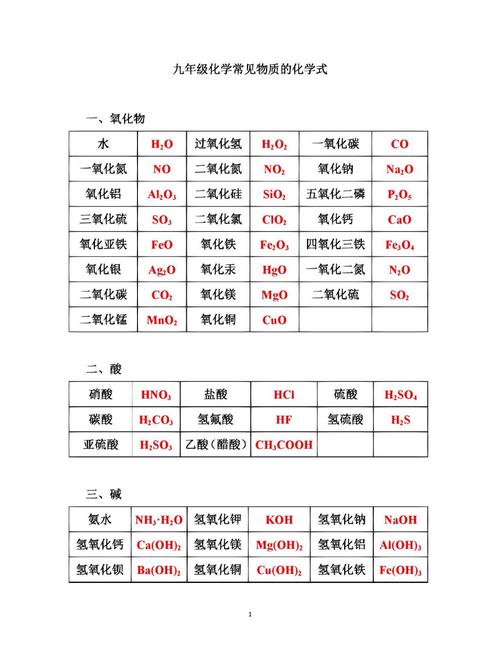
(1) 氧化物
定义:由两种元素组成,其中一种是氧元素的化合物。
| 分类 | 定义 | 举例 | 性质 |
|---|---|---|---|
| 酸性氧化物 | 能与碱反应生成盐和水的氧化物,非金属氧化物大多是酸性氧化物。 | 二氧化碳(CO₂)、二氧化硫(SO₂) | 溶于水一般能形成酸,如 CO₂ + H₂O → H₂CO₃ (碳酸) |
| 碱性氧化物 | 能与酸反应生成盐和水的氧化物,金属氧化物大多是碱性氧化物。 | 氧化铜、氧化钙、氧化铁 | 溶于水一般能形成碱,如 CaO + H₂O → Ca(OH)₂ (氢氧化钙) |
| 两性氧化物 | 既能与酸反应,又能与碱反应生成盐和水。 | 氧化铝(Al₂O₃)、氧化锌 | - |
(2) 酸
定义:电离时产生的阳离子全部是氢离子(H⁺)的化合物。

(图片来源网络,侵删)
| 分类标准 | 类别 | 举例 | 特点 |
|---|---|---|---|
| 电离出的H⁺个数 | 一元酸 | 盐酸、硝酸(HNO₃) | 1个H⁺ |
| 二元酸 | 硫酸(H₂SO₄)、碳酸(H₂CO₃) | 2个H⁺ | |
| 三元酸 | 磷酸(H₃PO₄) | 3个H⁺ | |
| 酸根是否含氧 | 含氧酸 | 硫酸(H₂SO₄)、硝酸(HNO₃) | 酸根中含有氧原子 |
| 无氧酸 | 盐酸(HCl)、氢硫酸(H₂S) | 酸根中不含氧原子 |
酸的通性(以稀盐酸、稀硫酸为例):
- 使紫色石蕊试液变红,无色酚酞不变色。
- 与活泼金属反应生成盐和氢气。(如:Zn + H₂SO₄ → ZnSO₄ + H₂↑)
- 与金属氧化物(碱性氧化物)反应生成盐和水。(如:CuO + 2HCl → CuCl₂ + H₂O)
- 与碱发生中和反应生成盐和水。(如:NaOH + HCl → NaCl + H₂O)
- 与某些盐反应生成新酸和新盐。(如:AgNO₃ + HCl → AgCl↓ + HNO₃)
(3) 碱
定义:电离时产生的阴离子全部是氢氧根离子(OH⁻)的化合物。
| 分类标准 | 类别 | 举例 | 特点 |
|---|---|---|---|
| 溶解性 | 可溶性碱 | 氢氧化钠、氢氧化钾、氢氧化钙、氢氧化钡 | 易溶于水,水溶液能使酚酞变红,石蕊变蓝。 |
| 难溶性碱 | 氢氧化铜、氢氧化铁、氢氧化镁 | 不溶于水,但具有碱的通性(如与酸反应)。 | |
| 微溶性碱 | 氢氧化钙 | 微溶于水。 |
碱的通性(以可溶性碱如NaOH、Ca(OH)₂为例):
- 使紫色石蕊试液变蓝,无色酚酞变红。
- 与非金属氧化物(酸性氧化物)反应生成盐和水。(如:2NaOH + CO₂ → Na₂CO₃ + H₂O)
- 与酸发生中和反应生成盐和水。(如:2HCl + Ca(OH)₂ → CaCl₂ + 2H₂O)
- 与某些盐反应生成新碱和新盐。(如:CuSO₄ + 2NaOH → Cu(OH)₂↓ + Na₂SO₄)
(4) 盐
定义:由金属阳离子(或铵根离子NH₄⁺)和酸根阴离子构成的化合物。
| 分类方式 | 类别 | 举例 |
|---|---|---|
| 按酸根 | 含氧酸盐 | 碳酸钠(Na₂CO₃)、硫酸铜(CuSO₄) |
| 无氧酸盐 | 氯化钠、氯化钙 | |
| 按组成 | 正盐 | 最常见的盐,酸中的氢离子完全被中和,如 NaCl, CaCO₃ |
| 酸式盐 | 酸中的氢离子部分被中和,如 NaHCO₃ (碳酸氢钠), Ca(HCO₃)₂ | |
| 碱式盐 | 碱中的氢氧根部分被中和,如 Cu₂(OH)₂CO₃ (碱式碳酸铜) |
盐的化学性质(举例):
- 与某些金属反应生成新盐和新金属。(如:Fe + CuSO₄ → FeSO₄ + Cu,注意“前置后”)
- 与酸反应生成新盐和新酸。(如:CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑)
- 与碱反应生成新盐和新碱。(如:CuSO₄ + 2NaOH → Cu(OH)₂↓ + Na₂SO₄)
- 与另一种盐反应生成两种新盐。(如:BaCl₂ + Na₂SO₄ → BaSO₄↓ + 2NaCl)
混合物的分类
混合物根据其均匀性,分为均一混合物和非均一混合物。
| 分类 | 定义 | 特点 | 举例 |
|---|---|---|---|
| 均一混合物 | 各部分的性质、组成完全相同。 | 外观均匀,肉眼无法区分其组成部分。 | 溶液(如食盐水、糖水、碘酒)、合金(如钢) |
| 非均一混合物 | 各部分的性质、组成不相同。 | 外观不均匀,可以清晰地看出不同的物质。 | 悬浊液(如泥水)、乳浊液(如牛奶)、空气(宏观均一,微观非均一) |
总结与记忆技巧
-
抓住核心标准:
- 纯净物 vs. 混合物:看物质种类(一种 vs. 多种)。
- 单质 vs. 化合物:看元素种类(一种 vs. 不同种)。
- 酸、碱、盐:看电离出的离子(H⁺ vs. OH⁻ vs. 金属离子+酸根离子)。
-
利用口诀记忆:
- 氧化物分类:“非成酸,金成碱” (非金属氧化物大多成酸,金属氧化物大多成碱)。
- 酸碱盐通性:记住它们之间可以相互反应,特别是酸和碱的中和反应是重点。
- 金属活动性顺序:“钾钙钠镁铝、锌铁锡铅氢、铜汞银铂金”,这是判断金属与酸、盐溶液反应的基础。
-
联系实际:生活中的物质很多都是混合物(如空气、饮料),而实验室用的药品大多是纯净物,将分类知识与生活实际联系起来,会更容易理解和记忆。
希望这份详细的梳理能帮助你系统地掌握九年级化学的物质分类!



